Как изменится объем газа в цилиндре если уменьшить объем газа
Добавил пользователь Евгений Кузнецов Обновлено: 04.10.2024
Как изменится давление газа в цилиндре , если уменьшить объем газа, переместив поршень на половину высоты цилиндра?
Как изменится давление газа в цилиндре , если уменьшить объем газа, переместив поршень на половину высоты цилиндра?
Температура газа постоянна.
значит давление нужно в 2 раза увеличить.
При сжатии идеального газа объем уменьшился в 2 раза и температура газа увеличилась в 2 раза ?
При сжатии идеального газа объем уменьшился в 2 раза и температура газа увеличилась в 2 раза .
Как изменилось при этом давление газа?
Давление идеального газа уменьшилось от 800кПа до 160кПа при постоянной температуре?
Давление идеального газа уменьшилось от 800кПа до 160кПа при постоянной температуре.
Во сколько раз увеличился объем газа?
Маса газа постоянна.
Изменилась ли масса воздуха в цилиндре под поршнем, если поршень вдвинули в цилиндр и газ стал занимать объем в два раза меньше первоначального?
Изменилась ли масса воздуха в цилиндре под поршнем, если поршень вдвинули в цилиндр и газ стал занимать объем в два раза меньше первоначального?
Разрешенный углекислый газ изображено занимается?
Разрешенный углекислый газ изображено занимается.
Масса газа постоянна.
Как надо изменить абсолютную температуру газа, чтобы уменьшить его объем в 4 раза?
Во сколько раз изменилась плотность газа , если давление газа в изотермическом процессе уменьшилось на 20%?
Во сколько раз изменилась плотность газа , если давление газа в изотермическом процессе уменьшилось на 20%?
Масса газа постоянна.
Объем сосуда с идеальным газом уменьшили вдвое, выпустив половину газа и поддерживая температуру газа в сосуде постоянной?
Объем сосуда с идеальным газом уменьшили вдвое, выпустив половину газа и поддерживая температуру газа в сосуде постоянной.
Как изменилась в результате этого давление газа в сосуде, его плотность и внутренняя энергия?
Газ находится в цилиндре под поршнем?
Газ находится в цилиндре под поршнем.
Какое положение займет поршень, если при уменьшении абсолютной температуры в 2 раза давление уменьшится в 3 раза?
Поршень массой 3кг и площадью 0, 1дм2 давит на газ в вертикальном цилиндре?
Поршень массой 3кг и площадью 0, 1дм2 давит на газ в вертикальном цилиндре.
Во сколько раз уменьшится объем газа, если на поршень поставить груз массой 3, 1кг?
Атмосферное давление 100кПа.
В цилиндре с газом посередине находится подвижный поршень?
В цилиндре с газом посередине находится подвижный поршень.
Что можно сказать о давлении газа слева и справа от поршня, если поршень неподвижен?
Газ находится в цилиндре с подвижным порншем и при температуре 300К занимает объем 250см3?
Газ находится в цилиндре с подвижным порншем и при температуре 300К занимает объем 250см3.
Какой объем займет газ, если температура понизится до 270К ?
На этой странице находится вопрос Как изменится давление газа в цилиндре , если уменьшить объем газа, переместив поршень на половину высоты цилиндра?, относящийся к категории Физика. По уровню сложности данный вопрос соответствует знаниям учащихся 10 - 11 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Физика. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.
Видео- Решение задач-теория
Так как температура газа не меняется, следовательно это изотермический процесс.
Пусть , тогда
Пусть , тогда
- закон Бойля - Мариотта: для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно.
Рассмотрим уравнения (1) и (2):
(1)
(2)
Подставим данные задачи для P2 и V2 в уравнение (1):
Подставим данные задачи для P3 и V3 в уравнение (2):
(1)
(2)
Выразим из уравнения (1) V1:
(3)
Подставим уравнение (3) в последнее уравнение (2), получим:
Ответ: начальное давление газа равно 400 Па.
2 - Определите температуру газа, находящегося в закрытом сосуде, если при нагревании газа на 1 °С его давление увеличится на 0,25% от первоначального.
Решение:
Так как сосуд закрыт, то объем газа не меняется. Следоваьельно это изохорный процесс.
- закон Шарля для изохорного процесса.
- (1)
- по условию задачи.
- по условию задачи.
Подставляем значения для P2 и T2 в уравнение (1), получим:
Ответ: температура газа равна 400 °С.
3 - Масса газа m при давлении имеет температуру T. Как изменится объем газа, если при уменьшении давления в 5 раз его температура увеличится до 2T, при этом 20 % газа улетучится?
Решение:
Пусть m1, T1, P1 - первоначальные масса, температура и давление газа.
- давление второго состояния газа.
- температура второго состояния газа.
- масса второго состояния газа.
- уравнение Клапейрона - Менделеева (уравнение состояния идеального газа, связывающее три макроскопические параметры: объем, давление и температуру газа данной массы).
(1) - уравнение Клапейрона - Менделеева для первого сотояния газа.
(2) - уравнение Клапейрона - Менделеева для второго состояния газа.
Подставим в уравнение (2) данные задачи.
(3)
Разделим уравнение (3) на уравнение (1), получим:
Ответ: объем увеличится в 8 раз.
4 - Определите давление воздуха в камере сгорания дизельного двигателя при температуре 512 °C, если плотность воздуха равна 1,8 кг/м 3 .
Решение:
- уравнение Клапейрона - Менделеева (уравнение состояния идеального газа, связывающее три макроскопические параметры: объем, давление и температуру газа данной массы).
- связь температур по шкале Цельсия и Кельвина.
- формула для массы газа, где V - объем, ρ - плотность газа.
- выражаем давление из уравнения Клапейрона - Менделеева.
- молярная масса воздуха.
Ответ: P=4 МПа.
5 - Газ массой 24 г при температуре 112 °C и давлении 2 МПа занимает объем 1,2 л. Определите молярную массу газа.
Решение:
- связь температур по шкале Цельсия и Кельвина.
- уравнение Клапейрона - Менделеева (уравнение состояния идеального газа, связывающее три макроскопические параметры: объем, давление и температуру газа данной массы).
- выражаем молярную массу из уравнение Капейрона - Менделеева.
Ответ: .
6 - Как изменится абсолютная температура идеального газа при уменьшении его объема в 2 раза и увеличении давления в 3 раза?
Решение:
- уравнение Клапейрона - Менделеева (уравнение состояния идеального газа, связывающее три макроскопические параметры: объем, давление и температуру газа данной массы).
- объем уменьшился в 2 раза.
- давление увеличилось в 3 раза.
Ответ: абсолятная температура идеального газа приуменьшении его объема в 2 раза и увеличении давления в 3 раза увеличится в 1,5 раза.
7 - При какой температуре средняя квадратичная скорость электрона равна 2*10 5 м/с?
Решение:
- масса электрона.
- постоянная Больцмана.
- средняя кинетическая энергия молекулы, где ma - масса молекулы, - средняя квадратичная скорость молекулы.
.
.
Ответ: при температуре 4,3*10 -3 K средняя квадратичная скорость электрона равна 2*10 5 м/с.
8 - Как изменится давление идеального газа, если при неизменной концентрации средняя квадратичная скорость молекул увеличится в 2 раза?
Решение:
- основное уравнение молекулярно-кинетической теории идеального газа, где p - давление газа, n - концентрация молекул, - средняя кинетическая энергия молекулы, - масса молекулы.
Как изменится объем газа в цилиндре если уменьшить объем газа
С1-1. На полу неподвижного лифта стоит теплоизолированный сосуд, открытый сверху. В сосуде под тяжёлым подвижным поршнем находится одноатомный идеальный газ. Поршень находится в равновесии. Лифт начинает равноускоренно опускаться вниз. Опираясь на законы механики и молекулярной физики, объясните, куда сдвинется поршень относительно сосуда после начала движения лифта и как при этом изменится температура газа в сосуде. Трением между поршнем и стенками сосуда, а также утечкой газа из сосуда пренебречь.
С1-2. В цилиндре, закрытом подвижным поршнем, находится идеальный газ. На рисунке показана диаграмма, иллюстрирующая изменение внутренней энергии U газа и передаваемое ему количество теплоты Q. Опишите изменение объема газа при его переходе из состояния 1 в состояние 2, а затем в состояние 3. Свой ответ обоснуйте, указав, какие физические закономерности вы использовали для объяснения.
С1-2. В цилиндре, закрытом подвижным поршнем, находится идеальный газ. На рисунке показана диаграмма, иллюстрирующая изменение внутренней энергии U газа и передаваемое ему количество теплоты Q. Опишите изменение объема газа при его переходе из состояния 1 в состояние 2, а затем в состояние 3. Свой ответ обоснуйте, указав, какие физические закономерности вы использовали для объяснения.
С1-3. В цилиндре, закрытом подвижным поршнем, находится газ, который может просачиваться сквозь зазор вокруг поршня. В опыте по изотермическому сжатию газа его объем уменьшился вдвое, а давление газа упало в 3 раза. Во сколько раз изменилась внутренняя энергия газа в цилиндре? (Газ считать идеальным.)
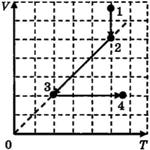
C1-5. Ha V T-диаграмме показано, как изменялись объём и температура некоторого постоянного количества разреженного газа при его переходе из начального состояния 1 в состояние 4. Как изменялось давление газа р на каждом из трёх участков 1—2, 2—3, 3—4: увеличивалось, уменьшалось или же оставалось неизменным? Ответ поясните, указав, какие физические явления и закономерности вы использовали для объяснения.
C1-6. В цилиндрическом сосуде под поршнем длительное время находятся вода и ее пар. Поршень начинают выдвигать из сосуда. При этом температура воды и пара остается неизменной. Как будет меняться при этом масса жидкости в сосуде? Ответ поясните, указав, какие физические закономерности вы использовали для объяснения.
С3-9. Нагреваемый при постоянном давлении идеальный одноатомный газ совершил работу 400 Дж. Какое количество теплоты было передано газу?
С3-11. В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 8 раз, давление воздуха в сосуде увеличилось в 2 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
С3-12. В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 4 раза, давление воздуха в сосуде увеличилось тоже в 4 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
С3-13. С разреженным азотом, который находится в сосуде под поршнем, провели два опыта. В первом опыте газу сообщили, закрепив поршень, количество теплоты Q1 = 742 Дж, в результате чего его температура изменилась на некоторую величину ΔT. Во втором опыте, предоставив азоту возможность изобарно расширяться, сообщили ему количество теплоты Q2 = 1039 Дж, в результате чего его температура изменилась также на ΔT. Каким было изменение температуры ΔT в опытах? Масса азота m = 1 кг.
С3-14. С разреженным азотом, который находится в сосуде под поршнем, провели два опыта. В первом опыте газу сообщили, закрепив поршень, количество теплоты Q1 = 742 Дж, в результате чего его температура изменилась на 1 К. Во втором опыте, предоставив азоту возможность изобарно расширяться, сообщили ему количество теплоты Q2 = 1039 Дж, в результате чего его температура изменилась также на 1 К. Определите массу азота в опытах.
С3-15. В горизонтальном цилиндрическом сосуде, закрытом поршнем, находится одноатомный идеальный газ. Первоначальное давление p = 4 • 10 5 Па. Расстояние от дна сосуда до поршня L = 30 см. Площадь поперечного сечения поршня S = 25 см 2 . В результате медленного нагревания газа поршень сдвинулся на расстояние х = 10 см. При движении поршня на него со стороны стенок сосуда действует сила трения величиной Fтр = 3•10 3 H. Какое количество теплоты получил газ в этом процессе? Считать, что сосуд находится в вакууме.
С3-16. В горизонтальном цилиндрическом сосуде, закрытом подвижным поршнем, находится одноатомный идеальный газ. Давление окружающего воздуха р = 10 5 Па. Трение между поршнем и стенками сосуда пренебрежимо мало. В процессе медленного охлаждения от газа отведено количество теплоты │Q│ = 75 Дж. При этом поршень передвинулся на расстояние х = 10 см. Чему равна площадь поперечного сечения поршня? Количество вещества газа постоянно.
С3-17. В горизонтальном цилиндрическом сосуде, закрытом поршнем, находится одноатомный идеальный газ. Первоначальное давление газа р1 = 4 · 10 5 Па. Расстояние от дна сосуда до поршня равно L. Площадь поперечного сечения поршня S = 25 см 2 . В результате медленного нагревания газ получил количество теплоты Q = 1,65 кДж, а поршень сдвинулся на расстояние х = 10 см. При движении поршня на него со стороны стенок сосуда действует сила трения величиной Fтp = 3 · 10 3 Н. Найдите L. Считать, что сосуд находится в вакууме.
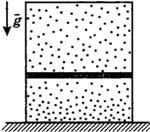
С3-18.Вертикальный замкнутый цилиндрический сосуд высотой 50 см разделен подвижным поршнем весом 110 Н на две части, в каждой из которых содержится одинаковое количество идеального газа при температуре 361 К. Сколько молей газа находится в каждой части цилиндра, если поршень находится на высоте 20 см от дна сосуда? Толщиной поршня пренебречь.
С3-19.В вертикальном теплоизолированном цилиндрическом сосуде под поршнем находится 0,5 моль гелия, нагретого до некоторой температуры. Поршень сначала удерживают, затем отпускают, и он начинает подниматься. Масса поршня 1 кг. Какую скорость приобретет поршень к моменту, когда поршень поднимется на 4 см, а гелий охладится на 20 К? Трением и теплообменом с поршнем пренебречь.
С3-20. Теплоизолированный сосуд объемом V = 2 м 3 разделен теплоизолирующей перегородкой на две равные части. В одной части сосуда находится 2 моль Не, а в другой — такое же количество моль А r . Температура гелия Т1 = 300 К, а температура аргона Т2 = 600 К. Определите парциальное давление аргона в сосуде после удаления перегородки.
Термодинамика С3-21. На рисунке изображено изменение состояния 1 моль идеального одноатомного газа. Начальная температура газа 27° С. Какое количество теплоты сообщено газу в этом процессе?
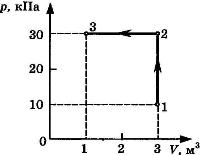
С3-23. На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
С3-24. На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
С3-25. На диаграмме (см. рисунок) представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
Задание 12. МКТ, термодинамика. Установление соответствия . ЕГЭ 2022 по физике

С некоторой массой идеального газа был проведён циклический процесс, изображённый на рисунке. Укажите, как менялся объём газа при переходе из 1 → 2 и 4 → 1. Для каждого случая определите соответствующий характер изменения:
| Процессы | Характер изменения |
| A) Процесс 1 → 2 Б) Процесс 4 → 1 | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждого процесса. Цифры в ответе могут повторяться.
Решение
В процессе 1-2 объем газа не менялся, т.к. переход 1-2 - это изохора, покольку его продолжение идет через начало координат. Переход 4-1 - изобара, т.к. $p_1=p_4$, тогда $
Задача 10
В сосуде объёмом V при давлении p и температуре T находится идеальный газ массой m и молярной массой M . Установите соответствие между физическими величинами и формулами, по которым их можно рассчитать.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите выбранные цифры под соответствующими буквами.
| Физические явления | Формулы |
| А) давление газа Б) температура газа | 1) $ 2) $ 3) $ 4) $ |
Решение
Из формул и формулировок МКТ очевидно, что $P=
Задача 11
По мере понижения температуры воды от +40◦С до −20◦С она находилась сначала в жидком состоянии, затем происходил процесс её отвердевания и дальнейшее охлаждение твёрдой фазы воды–льда. Изменялась ли внутренняя энергия воды во время этих процессов и если изменялась, то как? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Отвердевание воды Б) Охлаждение льда | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
1) Отвердевание воды и охлаждение льда два процесса, подчиняющихся первому началу термодинамики, согласно которому внутренняя энергия изменяется при совершении работы или передачи тепла. Следовательно, внутренняя энергия воды уменьшилась в ходе всех двух процессов.
Задача 12
В цилиндрическом сосуде под поршнем находится газ. Поршень может перемещаться в сосуде без трения. На дне сосуда лежит шарик. Из сосуда выпускается половина газа при неизменной температуре. Как изменились в результате этого объём газа и действующая на шарик архимедова сила? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Объём газа Б) Архимедова сила | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
Если у сосуда выпустить половину газа, то атмосферное давление уравновесит давление поршнем и поршень передвинется вниз, вследствие чего, объем газа уменьшится. Архимедова же сила, действующая на шарик, не изменится, поскольку плотность газа под поршнем останется неизменной: $F_<арх>=p_г·g·V_ш$, где $g=9.8м/с^2$ - ускорение свободного падения, $V_ш$ - объем шарика, $p_г$ - плотность газа под поршнем.
Задача 13
Температуру нагревателя тепловой машины уменьшили, оставив температуру холодильника прежней. Количество теплоты, полученное газом от нагревателя за цикл, не изменилось. Как изменились при этом КПД тепловой машины и количество теплоты, отданное газом за цикл холодильнику? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) КПД тепловой машины Б) Количество теплоты, отданное газом за цикл холодильнику | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
Если понизить температуру нагревателя при неизменной температуре холодильника, то КПД идеальной тепловой машины уменьшается в соответствие с уравнением: $η=(1-
Задача 14
Если налить воду в открытый сосуд, то она начнёт испаряться. Как будут меняться при этом её температура и внутренняя энергия? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Температура Б) Внутренняя энергия | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
При испарении, жидкость покидают наиболее быстрые молекулы, поэтому средняя скорость остальных молекул жидкости становится меньше. Следовательно, и средняя кинетическая энергия остающихся в жидкости молекул уменьшается. Это означает, что температура жидкости и внутренняя энергия испаряющейся жидкости уменьшается.
Задача 15
Ученик наблюдает за процессом кипения воды, нагреваемой в кастрюле на электроплите. Как в процессе кипения меняется температура и внутренняя энергия системы «вода–пар»? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Температура Б) Внутренняя энергия | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
При кипении, температура системы "вода-пар" остается постоянной, а внутренняя энергия данной системы увеличивается, т.к. происходит поглощение тепловой энергии.
Задача 16
В вертикальном цилиндрическом сосуде под поршнем, способным перемещаться без трения, находится воздух.Как изменятся температура газа и его объём, если поршень быстро сместить вниз? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Температура Б) Объём | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
Если поршень быстро сместить вниз, то объем газа уменьшится, давление - увеличится, а так как давление связано с температурой соотношением: $p=nkT$, то и температура тоже увеличится.
Задача 17
В вертикальном цилиндрическом сосуде под поршнем, способным перемещаться без трения, находится воздух. Как изменятся давление газа и его внутренняя энергия, если поршень быстро сместить вверх? Для каждой величины определите соответствующий характер изменения:
| Физические величины | Характер изменения |
| A) Давление Б) Внутренняя энергия | 1) увеличится 2) уменьшится 3) не изменится |
Запишите выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Решение
Если поршень сместить вверх, то обмен с окружающейс средой произойти не успеет - процесс будет адиабатным. Тогда из 1 закона термодинамики $Q=0=A+∆U$, тогда $∆U=-A$. Газ расширяется, значит $A>0$, следовательно, и $∆U T_1$, то при повышении температуры воздуха скорость его молекул увеличится, это приведет к увеличению ударов молекул о стенки сосуда и поршня, а следовательно, к увеличению давления, что приведет к тому, что поршень сместится, увеличив объем газа, плотность же газа, уменьшится, поскольку $p=
Идеальный газ
Задачи на эту тему кому-то могут показаться чуть более сложными, но вместе разберемся!
1.Как изменится температура идеального газа заданной массы, если его объем уменьшить вдвое, а давление вдвое увеличить?
2. При повышении абсолютной температуры идеального газа в 2 раза давление газа увеличилось на 25%. Во сколько раз при этом изменился объем?
Решение аналогично предыдущей задаче: опять воспользуемся уравнением состояния идеального газа , только выразим из него объем газа, для этого опять заменим концентрацию на : , или , откуда /p" />
. Запишем изменения давления и температуры: , . Изменение объема можно записать как отношение: /
.
Подставляем: /
, то есть объем увеличился в 1,6 раза.
3. При уменьшении объема газа в два раза давление увеличилось на 120 кПа и абсолютная температура возросла на 10%. Каким было первоначальное давление?
Запишем изменение давления: , объема " />
и температуры: , Запишем отношение давлений, для этого воспользуемся уравнением состояния идеального газа: /V" />
. Отношение давлений: /
. Теперь обратимся к давлениям: =5/11" />
. Это простое линейное уравнение, перепишем его: . Тогда , откуда кПа.
4. Газ при давлении 0,2 МПа и температуре C" />
имеет объем 5 л. Чему равен объем газа этой массы при нормальных условиях?
5. Укажите среднеквадратичную скорость движения молекул неона при температуре 150 К.
6. На рисунке изображен циклический процесс 1-2-3-4-1, совершаемый над идеальным газом. Можно утверждать, что
1) на участке 1-2 газ работу не совершает
2) на участке 4-1 внутренняя энергия газа увеличивается
3) на участке 1-2 газу сообщают некоторое количество теплоты
4) на участке 2-3 газ совершает положительную работу
7. В таблице указана плотность газов при нормальном атмосферном давлении.
| Газ | Плотность газа, кг/м.куб |
|---|---|
| Азот | 1,25 |
| Водород | 0,09 |
| Ксенон | 5,9 |
| Хлор | 3,2 |
При этом наибольшую среднеквадратичную скорость имеют молекулы
1) азота
2) водорода
3) ксенона
4) хлора
Так как среднеквадратичная скорость =sqrt<<3kT>/m_0>" />
зависит от массы молекулы , а значит, от молярной массы, то чем больше молярная масса (знаменатель), тем меньше скорость. Осталось найти из предложенных газ с наименьшей молярной массой: это водород.
8. В закрытом сосуде с сухими стенками воздух немного нагрели. Как при этом изменились концентрация молекул воды и относительная влажности воздуха в сосуде?
1) и концентрация молекул, и относительная влажность уменьшились
2) концентрация увеличилась, а относительная влажность не изменилась
3) концентрация уменьшилась, а относительная влажность увеличилась
4) концентрация не изменилась, а относительная влажность уменьшилась

9. В каком из четырех состояний, показанных для некоторой массы идеального газа точками на pV –диаграмме, идеальный газ обладает максимальной внутренней энергией?
Изопроцессы - МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ
Цель урока: рассмотреть частные случаи закона Клапейрона.
I. Проверка домашнего задания. Повторение изученного
1. Каковы нормальные условия для идеального газа?
2. Какова концентрация молекул идеального газа при нормальных условиях?
3. Какие макроскопические параметры связывает уравнение Клапейрона-Менделеева?
4. Какие параметры необходимо знать для определения состояния идеального газа?
II. Самостоятельная работа
1. Как изменится давление идеального одноатомного газа при уменьшении его объема в 4 раза и увеличении абсолютной температуры в 2 раза?
А. Увеличится в 8 раз.
Б. Увеличится в 4 раза.
В. Увеличится в 2 раза.
2. Вычислите давление кислорода массой 0,032 кг в сосуде объемом 8,3 м 3 при температуре 100 °С.
3. Как меняется масса воздуха в помещении, если температура увеличивается?
В. Не изменяется.
4. Чему равен объем 1 моля идеального газа при нормальных условиях?
5. В баллоне находится газ при t = 27 °С. Во сколько раз уменьшится давление газа, если 50 % его выйдет из баллона, а температура при этом увеличится до 600 К?
6. Масса кислорода m при давлении Р занимает объем V. Как изменится температура газа, если при увеличении давления до 2Р его объем уменьшился в V/10?
A. Увеличится в 5 раз.
Б. Уменьшится в 5 раз.
7. В баллоне при неизменной массе газа температура увеличилась от 1 до 2 °С. Как изменилось давление?
A. Увеличилось в 2 раза.
Б. Увеличилось в 1,004 раза.
B. Не изменилось.
8. Что и по каким физическим величинам можно вычислить на основании уравнения Менделеева-Клапейрона?
1. Плотность газа, используя R, р, Т, М.
2. Число молекул в газе, используя V, Т, Р, с.
3. Массу молекулы, используя Т, Р, с, NA, R.
1. Как изменится давление идеального одноатомного газа при увеличении его объема и температуры в 2 раза?
A. Увеличится в 4 раза.
Б. Уменьшится в 2 раза.
B. Останется прежним.
2. Вычислите давление водорода массой 0,02 кг в сосуде объемом 8,3 м 3 при температуре 100 °С.
3. Как изменится плотность воздуха в помещении, если температура уменьшится?
4. Чему равны давление и температура газа при нормальных условиях?
A. р = 10 5 Па·t – 100 °С 1 м 3 .
Б. р = 10 5 Па·Т - 273 К.
B. р = 10 5 кПа·T - 273 К.
5. В баллоне находится газ при Т = 300 К. Во сколько раз уменьшится давление газа, если 50 % его выйдет из баллона, а температура останется неизменной?
A. Уменьшится в 50 раз.
Б. Уменьшится в 2 раза.
B. Увеличится в 2 раза.
6. При нормальных условиях плотность кислорода:
A. Больше плотности водорода.
Б. Меньше плотности водорода.
B. Равна плотности водорода.
7. При повышении температуры в комнате меняется:
Б. Давление и масса воздуха.
B. Масса воздуха.
8. В цилиндре с поршнем произошло увеличение давления газа больше допустимого за счет увеличения температуры. Как можно установить прежнее давление?
A. Увеличением объема цилиндра или уменьшением массы газа.
Б. Только уменьшением массы газа.
B. Только увеличением объема цилиндра.
Ответы к самостоятельной работе
Ответы и номера вопросов
III. Изучение нового материала
Если одновременно меняются все характеристики состояния газа, то трудно установить какие-либо закономерности. Прошу изучить процессы, в которых масса и один из трех параметров - р, V или Т остаются неизменными.
Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами.
Первый газовый закон был открыт английским ученым Р. Бойлем (1627- 1691 гг.) в 1600 г. Работа называлась «Новые эксперименты, касающиеся воздушной пружины». Бойль изучал изменение давления газа в зависимости от объема при постоянной температуре. Данный процесс называется изотермическим.
Независимо от Бойля несколько позднее французский ученый Э. Мариотт пришел к тем же выводам. Поэтому закон получил название Бойля-Мариотга.
Закон Гей-Люссака (1802 г.)
Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным.
Объем данной массы газа при p = const зависит от температуры по лин. закону
Закон Ж. Шарля (1787 г)
При V = const давление данной массы газа при постоянном объеме зависит от температуры по линейному закону:
Фронтальное экспериментальное задание 1
«Наблюдение зависимости объема данной массы газа от температуры при постоянном давлении»
Приборы и материалы: 1) пробирка химическая, закрытая пробкой со стеклянной трубной длиной 150-200 мм, диаметром 4-5 мм; 2) стакан низкий с водой.
1. Подготовьте оборудование для опыта. Для этого опустите конец трубки с пробкой в стакан с водой на глубину 3-4 см, закройте пальцем другой конец и выньте трубку из воды. Расположите трубку горизонтально. Осторожно закройте пробирку пробкой так. чтобы столбик воды не вылился из трубки.
2. Нагрейте воздух в пробирке, подержав ее несколько секунд в руке. При этом наблюдайте за положением столбика воды в трубке.
3. Прекратите нагревание воздуха в пробирке и снова в течение нескольких секунд, наблюдайте за изменением положения столбика воды в трубке.
4. Ответьте на вопросы:
- Зависимость между какими величинами вы наблюдали на опыте?
- Изменялись ли давление и масса воздуха в пробирке во время опыта?
- Что можно сказать о зависимости объема данной массы воздуха от температуры при постоянном давлении?
Фронтальное экспериментальное задание 2
«Наблюдение зависимости давления данной массы газа от температуры при постоянном объеме»
Тест по физике Уравнение Клапейрона-Менделеева для 10 класса
Тест по физике Уравнение Клапейрона-Менделеева. Изотопы для 10 класса с ответами. Тест включает в себя 2 варианта. В каждом варианте по 5 заданий.
1 вариант
1. Как изменится давление идеального газа при увеличении температуры и объема газа в 4 раза?
А. Увеличится в 4 раза
Б. Уменьшится в 4 раза
В. Не изменится
2. В одинаковых сосудах при одинаковой температуре находятся водород (Н2) и углекислый газ (СО2). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки сосуда?
А. Водород в 22 раза
Б. Углекислый газ в 22 раза
В. Водород в 11 раз
3. Какому процессу соответствует график, изображенный на рисунке 26?
А. Изохорному
Б. Изобарному
В. Изотермическому
4. Во сколько раз изменится давление воздуха в цилиндре (рис. 27), если поршень переместить на l/3 влево?
А. Не изменится
Б. Увеличится в 1,5 раза
В. Уменьшится в 1,5 раза
5. Во сколько раз отличается плотность метана (СН4) от плотности кислорода (O2) при одинаковых условиях?
А. Плотность метана в 2 раза меньше
Б. Плотность метана в 2 раза больше
В. Плотность газов одинакова
2 вариант
1. Как изменится давление идеального газа при уменьшении температуры и объема газа в 2 раза?
А. Увеличится в 2 раза
Б. Не изменится
В. Уменьшится в 2 раза
2. В одинаковых баллонах при одинаковой температуре находятся кислород (O2) и метан (СН4). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки баллона?
А. Кислород в 2 раза
Б. Метан в 2 раза
В. Метан в 4 раза
3. Какому процессу соответствует график, изображенный на рисунке 28?
А. Изохорному
Б. Изотермическому
В. Изобарному
4. Во сколько раз изменится давление воздуха в цилиндре (рис. 29), если поршень переместить на l/3 вправо?
А. Не изменится.
Б. Увеличится в 1,33 раза
В. Уменьшится в 1,33 раза
5. До какой температуры при нормальном давлении надо нагреть кислород, чтобы его плотность стала равна плотности азота при нормальных условиях?
А. До 39 °С
Б. До 59 °С
В. До 29 °С
Ответы на тест по физике Уравнение Клапейрона-Менделеева. Изотопы для 10 класса
1 вариант
1-В
2-А
3-А
4-Б
5-А
2 вариант
1-Б
2-Б
3-В
4-В
5-А
Сжатие и расширение газов
Бойль нашел математическое соотношение между давлением и объемом данной массы газа. Однако Мариотт сделал существенное дополнение к его исследованием, в результате появился закон Бойля Мариотта. Суть его сводится к следующему: объем данной массы газа обратно пропорционален давлению при условии постоянства температуры. Другой способ выражения того же закона: произведение давления на объем есть величина постоянная для данной массы газа при неизменной температуре.
Формулы закона Бойля Мариотта
P1/P2=V2/V1
P1V1=P2V2
При пользовании этими формулами безразлично, в каких единицах вы будете измерять объем и давление, лишь бы оба объема и оба давления были измерены в одинаковых единицах. Например, если одно давление измерено в килограммах на квадратный сантиметр, то в тех же единицах должно быть измерено и другое давление. Если один объем измерен в кубических сантиметрах, то так же должен быть измерен и другой.
Применение закона Бойля Мариотта в быту
Пылесос состоит главным образом из вентилятора, приводимого в движение электромотором. Вентилятор выталкивает воздух своими лопастями и создает за ними разреженное пространство. Так как воздух, который из-за разности давлений внутри и снаружи устремляется по трубке в камеру вентилятора, проходит через ковер, то пыль уносится с ковра. В некоторых пылесосах применяется, кроме того, вращающаяся щетка, подметающая и выбивающая ковер. Воздух, прошедший вентилятор, поступает в мешок или другой отстойник для пыли и грязи, которые потом могут быть опорожнены различными способами в зависимости от типа пылесоса.
Водолазные колокола и водолазные костюмы. Когда водолазный колокол погружается в воду, воздух тоже сжимается, но при помощи компрессора, находящегося снаружи. Воздух нагнетается под колокол, поэтому вода совсем не входит в колокол. При этом необходимо все время накачивать в колокол свежий воздух в количестве, необходимом для работающих там людей. Излишек воздуха будет пузырями вырываться наружу. Важной частью водолазного костюма является шлем, который привинчивается к верхней части водонепроницаемого костюма. Обычно шлем снабжают воздухом таким же образом, как водолазный колокол. В некоторых типах костюмов водолаз имеет при себе собственный запас сжатого воздуха.
Одно из своеобразных проявлений закона Бойля — наше дыхание. Когда мускулы, сокращаясь, тянут диафрагму вниз, объем пространства, где помещаются легкие, увеличивается, отчего давление внутри становится меньше наружного. В результате воздух из пространства с большим давлением поступает в легкие, где давление меньше. Обратное движение диафрагмы уменьшает объем легочного пространства и делает давление внутри легких большим наружного. Поэтому воздух и ненужные газы выходят из легких.
Как изменится объем газа в цилиндре если уменьшить объем газа
По закону Бойля V1 : V2 = Р2 : P1 при постоянной температуре
По закону Гей-Люсака V1 : V2 = T1 : T2 при постоянном давлении
P1 : Р2 = T1 : T2 при постоянном объёме
Из формул, представленных выше, можно заметить, что две из трех величин, могут рассматриваться как переменные, если третья постоянна. Нет такого состояния, при котором давление, объем и температура могли бы все рассматриваться как переменные.
Однако бывают случаи, когда все величины переменные, а один фактор неизвестен. В практических случаях такие задачи могут быть решены по аналогии с примерами ниже:
Газ при температуре 20 o C занимает объем 0,98 м 3 в цилиндре диаметром 50 мм, к поршню приложена сила 980Н. Каким будет смещение поршня, если сила, приложенная к поршню, удвоилась, а температура увеличилась до 50 o C?
Смещение поршня легко определить при задании изменений объема. Однако, в задаче задано только одно значение объема (0,98 м 3 ), а другое неизвестно.
Чтобы установить зависимости между всеми параметрами, которые являются переменными, изменения объема должны быть рассмотрены отдельно при двух фазах.
Случай А 1-ая фаза
Газ нагревается от температуры t = 20 o C, которая соответствует абсолютной температуре T1 = 20 + 273 = 293 o K, до температуры 50 o C, которая соответствует T2 = (50 + 273) =323 o K. Если давление на поршень остается постоянным с нагрузкой 980Н, то произойдет увеличение объема газа. По закону Гей-Люсака V1 : V2 = T1 : T2
Подставляя заданные значения:
Vх = (0,98 • 323)/293 =1,08 дм 3 (промежуточное значение)
2-ая фаза
Газ, достигнув объема Vх = 1,08 дм 3 в результате увеличения температуры до T2 (323 o K), теперь получает дополнительное воздействие - увеличилась сила, приложенная к поршню. В результате, оно возрастает до P2 = 980 • 2 = 1960 Н, а объем уменьшается, поскольку воздух сжимается поршнем. По закону Бойля Vх : V2 = P2 : Р1 (Vх • P1 = V2 • P2)
Подставляя заданные значения:
V2 = (1,08 • 980)/1960 = 0,54 дм 3 (окончательное значение)
Отметим, что параметры P1 и Р2 были представлены как символы приложенной силы, а не единицы давления. Это - не ошибка, поскольку сила относится непосредственно к давлению в этом примере, так как диаметр поршня не изменяется.
Это подтверждается следующими вычислениями.
I. Площадь поверхности поршня в см 2 (3,14•D2)/4
Диаметр = 50 мм = 5 см S = (3,14 • 52)/4 = 19,6 см 2
Давление на каждой стадии теперь можно рассчитать.
II. Начальное давление P1=Начальная сила/Площадь поверхности = 980Н/19,6см 2 = 50Н/см 2 =5кг/см 2
Финальное давление P2= Финальная сила/Площадь поверхности = (980•2)/19,6 =100Н/см=10кг/см 2
При равенстве площадей поверхности поршня увеличение вдвое приложенной силы удвоит давление.
Подставляя заданные значения:
Vх • P1 = V2 • P2
V2 = (1,08 дм 3 • 50 Н/см 2 )/100Н/см 2 = (1,08 дм 3 • 5 кг/см 2 )/10кг/см 2 = 0,54 дм 3
Этот же самый результат получен в предыдущем вычислении.
Можно получить результат, непосредственно используя следующее выражение, которое является комбинацией из двух начальных формул:
(P 1 • V1)/Т1 = (P2 • V2)/Т2
В примере объем V2 требуется для того, чтобы вычислить перемещение поршня
V2 = (Р1 • V1 • T2)/(T1 • P2) = (5 • 0,98 • 323)/(293 • 10) = 0,54 дм 2
Используя оба объема, можно вычислить изменение в положении поршня, применяя геометрию:
Объем = площадь поверхности • высота Высота в см = объем в см 2 / площадь в см 2
Начальная высота = 980см 3 /19,6см 2 =50см. Финальная высота = 540см 3 /19,6см 2 =27,5см
Перемещение поршня = 50-27,5=22,5 см В этой задаче принималось, что нагревание газа произошло в результате увеличения температуры внешней среды.
Если вспомнить эксперимент с велосипедным насосом, когда воздух сжат и у него нет возможности расширяться, выделяется тепло, то есть температура воздуха возрастает и это тепло передается к внешним поверхностям насоса. Обратный процесс возникает, когда газ расширяется.
Если у газа есть возможность расшириться, его температура уменьшится.
Изменения температуры воздуха порождают:
I. Возникновение тепла на стадии сжатия.
II. Поглощение тепла на стадии расширения.
Изменения температуры могут быть рассчитаны, как показано, при использовании величин из предыдущего примера.
Количество газа при температуре 293°K занимает объем V1 =0,98 дм 3 при давлении 5 бар. Если давление повысить до 10 бар, объем уменьшится до V2=0,54 дм 3 .
Какой станет температура газа? Важно помнить, что закон Бойля работает только тогда, когда температура постоянна. Поэтому, при 293°K повышение давления от P1 до P2 приводит к уменьшению объема газа с V1 до Vх: V1 : Vх = P2 : P1 то есть. V1 • P1 = Vх • P2
Подставляя известные значения: Vх = (0,98 • 5)/10=0,49 дм 3
Используя закона Гей-Люсака и рассматривая давление как постоянную величину P2 (к которому уже отнесен объем Vх), можно записать:
Vх : V2 = Т1 : Т2 то есть Vх • T2 = V2 • T1
Подставляя известные значения: T2 = (0,54 • 293)/0,49 = 323°K Это значение равно значению, которое дано в начальном примере.
Читайте также:

