Очистка выхлопных газов от оксидов азота
Обновлено: 05.07.2024
СПОСОБ СЕЛЕКТИВНОЙ КАТАЛИТИЧЕСКОЙ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ОТ ОКСИДОВ АЗОТА В ПРОМЫШЛЕННЫХ УСТАНОВКАХ Российский патент 2007 года по МПК B01D53/56 B01D53/86 C01B21/20
Изобретение относится к технологии селективной очистки выхлопных газов от оксидов азота перед сбросом в атмосферу при помощи аммиака и преимущественно предназначено для очистки выхлопных газов в промышленных установках по производству азотной кислоты, но может быть использовано и в других промышленных установках и объектах энергетики.
В современных условиях каталитическая очистка выхлопных газов установок по производству азотной кислоты становится неотъемлемым элементом технологического процесса, обеспечивающая тонкую очистку до остаточного содержания NOx порядка 0,005 об.%.
В странах бывшего СССР все многочисленные установки по производству азотной кислоты были оборудованы такой очисткой.
В крупнотоннажных установках (УКЛ-7, АК-72) преобладали каталитические системы с высокотемпературной (700-760°С) очисткой при помощи природного газа, в установках с агрегатами малой мощности (по схеме 1/3,5 ата) - система селективной очисткой при помощи аммиака в диапазоне температур 250-280°С.
Источник информации - Справочник азотчика, том 2, Москва, Химия, 1987, стр.59-62, 65-92.
В последние годы селективная каталитическая очистка заменяет высокотемпературную очистку в агрегатах типа УКЛ-7, начался этот процесс и для реконструкции агрегатов типа АК-72. Это связано с рядом причин, но главное, что при этом достигается исключение или экономия катализатора, содержащего драгоценный металл (палладий) и резкое уменьшение содержания в выхлопных газах другого вредного вещества - окиси углерода (СО).
Как и высокотемпературный метод очистки природным газом, селективная очистка при помощи аммиака обеспечивает остаточное содержание NOx на уровне 0,005 об.%.
Широкое распространение селективного метода очистки при помощи чистого газообразного аммиака, который принят за прототип изобретения, заставляет обратить внимание на некоторые его недостатки:
- дополнительный расход аммиака (3-4 кг на 1 т HNO3);
- остаточное содержание NH3 в выхлопных газах (0,005-0,01 об.%), который в атмосфере может трансформироваться в NOx, и поэтому как вредное вещество приравнивается к NOx.
Последнее связано с необходимостью поддержания некоторого избытка NH3 против стехиометрии по отношению к NOx для обеспечения полноты очистки выхлопных газов от них. На величину избытка NH3 влияет несовершенство смешения газообразного аммиака с выхлопными газами перед реактором, соотношение объемов которых составляет ˜1:1000.
Увеличение расхода аммиака, хотя и незначительное (1,05-1,4%), увеличивает себестоимость азотной кислоты.
В существующем способе селективной каталитической очистки выхлопных газов, т.е. по прототипу, в смеситель перед реактором подают чистый газообразный аммиак под давлением, несколько превышающем давление выхлопных газов.
Поэтому в крупнотоннажных агрегатах типа АК-72 газообразный аммиак под нужным давлением (11-12 атм) вынуждены получать в специальной установке испарения жидкого аммиака водяным паром, что требует дополнительных капиталовложений и усложняет эксплуатацию.
Техническими задачами, на решение которых направлено настоящее изобретение, являются:
- улучшение смешения выхлопных газов с аммиаком (достижения гомогенности смеси) и вследствие этого уменьшение содержания в выхлопных газах непрореагировавшего аммиака;
- экономия энергоресурсов (электроэнергии, природного газа).
Согласно изобретению эти технические задачи решаются в совокупности путем смешения выхлопных газов со смесью аммиака с водородсодержащими газами. Такая смесь может либо составляться из газообразного аммиака, водорода или водородсодержащих газов, либо быть готовой смесью без дополнительного приготовления.
На предприятиях, где эксплуатируются установки по производству азотной кислоты, как правило, производится и аммиак.
Непрерывными отходами производства аммиака являются продувочные газы из цикла синтеза аммиака и танковые газы, выделяющиеся в сборниках при приеме из системы синтеза жидкого аммиака со сбросом давления до 20-40 атм.
Типовой состав продувочных газов на действующих производствах аммиака (АМ-70, АМ-76), об.%:
В агрегате аммиака мощностью 450-500 тыс.т/год количество продувочных газов колеблется в пределах 7500-8300 нм 3 /час.
В агрегате аммиака усредненно выделяется 1500-2000 нм 3 /час танковых газов.
Продувочные и танковые газы после вымораживания из них аммиака направляются на сжигание в смеси с природным газом в горелках печей риформинга производства аммиака, т.е. используются как топливо. При этом содержащийся в них аммиак теряется.
На отдельных установках аммиак из танковых газов отмывается водой с получением 15-20%-ной аммиачной воды.
Согласно настоящему изобретению, танковые и продувочные газы, содержащие аммиак, используется для селективной очистки выхлопных газов производства азотной кислоты в качестве готовых аммиак-водород-содержащих смесей.
В производствах азотной кислоты по схеме 1/3,5 ата и УКЛ-7 целесообразно использовать танковые газы, причем до вымораживания или частичного вымораживания аммиака в зависимости от мощности производства азотной кислоты.
Сущность и пример использования настоящего изобретения целесообразно проиллюстрировать применительно к производству азотной кислоты в агрегатах по схеме 7,3 ата (УКЛ-7), наиболее распространенных на предприятиях в России и странах СНГ.
Как типовой случай, на 1 агрегат аммиака мощностью 450-500 тыс.т/год на предприятии приходится 5 агрегатов УКЛ-7 с общей мощностью 600 тыс.т/год HNO3 или часовой - 5×14,8=74 т/час.
На 1 т HNO3 селективной очистке подлежат 3150-3200 нм 3 выхлопных газов с остаточным содержанием NOx после абсорбции 0,1 об.%. При степени окисленности NOx, равной 50%, в выхлопных газах содержится по 3175×0,001×0,5≈1,59 нм 3 NO и NO2.
Стехиометрический расход аммиака на восстановление NO и NO2 определяется реакциями:
Он составит 1,06+2,12=3,18 нм 3 на 1 т HNO3, а с избытком 5% для полноты очистки от NOx против стехиометрии - 3,34 нм 3 .
Часовая потребность в аммиаке для 5-ти агрегатов 3,34×74=247,2 нм 3 .
Танковые газы - отход от одного агрегата аммиака - содержат до вымораживания в среднем ˜1750×0,2=350 нм 3 NH3, т.е. часовая потребность в аммиаке для очистки выхлопных газов обеспечивается.
Количество и состав танковых газов на систему очистки выхлопных газов 5 агрегатов УКЛ-7 (по усредненному составу):
Состав смеси выхлопных газов с аммиаком перед реактором каталитической очистки (на 1 т HNO3):
Содержание Н2 и СН4 существенно ниже нижнего предела воспламенения этих горючих веществ в смесях даже с воздухом (4% для Н2 и 5,5% для CH4), тем более в смеси с содержанием инертов >95%.
Эффективность применения предлагаемого способа в агрегатах УКЛ-7 при их переводе на селективную очистку выхлопных газов повышается, если вместо обычно используемого ванадиевого катализатора АВК-10 применить алюмо-медь-цинковый катализатор АМЦ-10, разработанный для предотвращения ванадиевой коррозии нержавеющих сталей при температуре >600°С.
В отличие от катализатора АВК-10 на АМЦ-10 водород взаимодействует с кислородом при 250-280°С. В соответствии с тепловым балансом при указанном выше содержании водорода в смеси (0,17 об.%) можно получить прирост температуры до 20°С. Если применить танковый газ с более высокой выморозкой аммиака и соответственно с более высоким содержанием водорода, то это позволит или понизить предварительный подогрев выхлопных газов перед реактором селективной очистки на 30-50°С, и упростить этот узел с увеличением выхода пара, или поднять температуру выхлопных газов перед камерой сгорания турбины до 320°С (на 50°С), и несколько снизить удельный расход природного газа на 1 т HNO3, а также дополнительно высвободить воздух на получение HNO3.
В изложенном примере положительный эффект складывается из следующих составляющих:
- экономия аммиака - не менее 280 т/год на 5 агрегатов УКЛ-7 (который сжигается);
- улучшается гомогенность смеси выхлопных газов с аммиаком и снижается выброс аммиака в атмосферу;
- экономится искусственный холод (электроэнергия) на исключением вымораживания аммиака ˜80 тыс.кВтч.
В наибольшей степени эффективно использование предлагаемого способа при реконструкции агрегатов азотной кислоты АК-72 с переводом их на низкотемпературную селективную очистку с сохранением высокотемпературного реактора для нагрева выхлопных газов перед газовой турбиной до 740-760°С.
Дополнительно к положительному эффекту, описанному выше для реконструкции УКЛ-7, добавляется существенное улучшение условий эксплуатации подогревателя выхлопных газов ПВГ-1200 и возможность не увеличивать поверхность конвективной части подогревателя для достижения температуры выхлопных газов 300°С.
Это обуславливается возможностью повысить температуру выхлопных газов в реакторе селективной очистки за счет горения водорода на катализаторе АМЦ-10, который допускает повышение температуры до 320°С. Поэтому в конвективной части ПВГ-1200 можно ограничиться нагревом выхлопных газов до 270-280°С, получить нагрев до 320°С в реакторе. В результате снижается тепловая нагрузка радиационной части ПВГ-1200, расход природного газа за счет потерь тепла с выхлопными газами после ПВГ-1200, выбрасываемыми в атмосферу.
В агрегате АК-72 содержание NOX после абсорбции составляет 0,07 об.%.
Расход аммиака с 5%-ным избытком против стехиометрии - 2,34 нм 3 .
Чтобы в реакторе селективной очистки получить прирост температуры 40°С (от 280 до 320°С) содержание водорода должно составить ˜0,5%.
При указанных выше составах танковых, продувочных и выхлопных газов необходимо, как показывают расчеты, на 1 т HNO3 подать 7,91 нм 3 танковых газов и 22,1 нм 3 продувочных газов.
Количество и состав смеси танковых и продувочных газов на 1 т HNO3 следующий:
Часовой расход танковых газов 7,91×50≈400 нм 3 . Т.о., один агрегат аммиака типа АМ-70,76 обеспечивает потребность 2-х агрегатов АК-72.
Часовой расход продувочных газов 22,1×50≈1100 нм 3 , в т.ч. водорода ≈590 нм 3 .
Таким образом, обеспечиваются 2 агрегата АК-72.
При мембранном разделении продувочных газов и возврате водорода в цикл синтеза количество водорода в отходах от одного агрегата аммиака составляет ˜400 нм 3 /час. Поэтому для 2-х агрегатов АК-72 на этой стадии должен использоваться и продувочный газ до разделения.
Приведенными примерами не исчерпывается возможность предлагаемого способа. Эти примеры ограничены свойствами используемых на предприятиях отечественных катализаторов селективной очистки типа АВК-10 и АМЦ-10.
Так, на ванадиевом катализаторе АВК-10 водород в диапазоне рабочей температуры для этого катализатора 250-280°С не взаимодействует с кислородом. Если бы унос пыли катализатора не угрожал ванадиевой коррозией нержавеющей стали аппаратуре при температуре выше 600°С, то его применение позволило бы в агрегате АК-72 в полной мере использовать положительные стороны предлагаемого способа. А именно, позволило бы в выхлопной газ перед селективной очисткой подать значительно больше продувочных газов цеха синтеза аммиака, повысить содержание водорода в смеси до 2,5 об.%
Это дало бы возможность снизить температуру зажигания катализатора в высокотемпературном реакторе до 320-350°С и исключить необходимость догревать газ после реактора селективной очистки в радиационной части ПВГ-1200, что упростило бы схему этого узла и дало существенную дополнительную экономию природного газа.
Катализатор АМЦ-10 лишен этого недостатка АВК-10, но описанный выше процесс невозможно осуществить с его применением из-за ограничения по температуре (не более 320°С), а водород на этом катализаторе реагирует с кислородом с повышением температуры. Но так как можно ожидать создания других катализаторов селективной очистки, позволяющих повышать на них температуру процесса селективной очистки до ˜500°С при начальной температуре зажигания 250-300°С, то возможности предлагаемого способа будут использованы в более широком объеме, чем в приведенных выше примерах.
Необходимо отметить, что водород, являясь восстановителем, может частично участвовать в процессе селективной очистки наряду с аммиаком. Поэтому, помимо указанного выше положительного эффекта (экономия аммиака, природного газа, электроэнергии) техническое решение по настоящему изобретению позволяет ожидать дальнейшего снижения выброса вредных веществ в атмосферу за счет уменьшения остаточного содержания аммиака в выхлопных газах, не только вследствие улучшения качества смешения, но и вследствие того, что водород снимет необходимость поддерживать в смеси избыток аммиака против стехиометрического соотношения с NOx.
1. Справочник азотчика, том 2. Москва, Химия, 1987 г.
Похожие патенты RU2297272C2
- Ферд Максим Лейбович
- Юргенсон Николай Викторович
- Поплавский Виктор Юлианович
- Федорова Елена Максимовна
- Поплавский В.Ю.
- Федорова Е.М.
- Чернышев В.И.
- Бруштейн Е.А.
- Рябченко П.В.
- Дедов А.С.
- Дремов А.В.
- Захарова О.М.
- Логинов Н.Д.
- Мачехин Г.Н.
- Сеземин В.А.
- Шведов А.В.
- Шустов В.В.
- Шевченко В.В.
- Петров Н.Н.
- Каминский А.А.
- Чернышев В.И.
- Жигайло Б.Д.
- Зарубин В.М.
- Корчака Н.И.
- Антонов О.М.
- Грицив Р.Г.
- Шварцбурд И.Ю.
- Ферд М.Л.
- Иванов Ю.А.
- Янковский А.К.
- Коваленко Т.В.
- Караваев М.М.
- Иванов Ю.А.
- Кожевников А.О.
- Горшкова Надежда Васильевна
- Егорова Людмила Петровна
- Грошева Людмила Петровна
- Лагуткин Анатолий Петрович
- Поморцев Андрей Анатольевич
- Юргенсон Николай Викторович
- Ферд Максим Лейбович
- Миславская В.С.
- Чернышев В.И.
- Юргенсон Н.В.
- Ферд М.Л.
- Сквирский М.Е.
- Шустов В.А.
- Павелко В.З.
- Миславский Н.О.
- Чернышев Валерий Иванович
- Ященко Андрей Валерианович
- Шустов Владимир Анатольевич
- Ванчурин Виктор Илларионович
- Лоцман А.А.
- Караваев М.М.
- Иванов Ю.А.
- Пихтовников Б.И.
- Воробьев Ф.П.
Реферат патента 2007 года СПОСОБ СЕЛЕКТИВНОЙ КАТАЛИТИЧЕСКОЙ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ОТ ОКСИДОВ АЗОТА В ПРОМЫШЛЕННЫХ УСТАНОВКАХ
Изобретение относится к технологии очистки выхлопных газов от оксидов азота в промышленных установках с использованием селективной каталитической очистки при помощи аммиака. Способ включает восстановление оксидов азота аммиаком на катализаторе в присутствии водорода. Выхлопные газы смешивают перед подачей на катализатор с продувочными газами из цикла синтеза аммиака. Содержание водорода в смеси поддерживают ниже нижнего предела воспламенения. Продувочные газы обогащают аммиаком, смешивая их с танковыми газами синтеза аммиака. Изобретение снижает расходы аммиака, улучшает смешивание выхлопных газов с аммиаком, снижает выброс аммиака в атмосферу и расходы энергоресурсов. 1 з.п. ф-лы.
Формула изобретения RU 2 297 272 C2
1. Способ селективной каталитической очистки выхлопных газов от оксидов азота, включающий восстановление оксидов азота аммиаком на катализаторе в присутствии водорода, отличающийся тем, что выхлопные газы смешивают перед подачей на катализатор с продувочными газами из цикла синтеза аммиака, причем содержание водорода в смеси поддерживают ниже нижнего предела воспламенения. 2. Способ по п.1, отличающийся тем, что продувочные газы обогащают аммиаком, смешивая их с танковыми газами синтеза аммиака.
Очистка газов от оксидов азота
Методы очистки от оксидов азота основаны на их физико-химических свойствах. Разработаны окислительные, восстановительные, сорбционные и прочие методы. Классификация методов санитарной очистки газов от оксидов азота представлена на рисунке 6.7.
Окисление оксидов азота на низкотемпературных катализаторах. Окислительные методы санитарной очистки газов от NOxоснованы на предварительном окислении NO с последующим поглощением NO2 и N2Oразличными поглотителями. В промышленности используется метод гомогенного окисления в газовой фазе с помощью кислорода:
| 2 NO + O2 />2 N2O | (6.20) |
| NO + NO2 />N2O3 | (6.21) |
Скорость реакции окисления оксида азота газообразным кислородом увеличивается в присутствии твердых тел и некоторых катализаторов. Наибольшую активность проявляют катализаторы, приготовленные на основе драгоценных металлов. Исследована каталитическая активность различных типов материалов, которые оказывают не одинаковое действие на скорость окисления азота. По каталитической активности их условно разделяют на 3 группы.
Первая группа – инертные вещества, которые не оказывают влияния на скорость реакции окисления NO: полиэтилен, шамот, тзвестняк, динос, кокс, доломит, оксид алюминия, катализатор марки БАВ, НТК-4.
Вторая группа – вещества, обладающие малой каталитической активностью: кварцевое стекло, полистирол, железная и марганцевая руда, катализатор марки ГИАП-10, стекловолокно.
Наиболее активны катализаторы третьей группы: кокс, промотированный солями марганца, меди, фосфора, стекло, алюмогель, уголь из абрикосовых косточек, силикагель, карбоалюмогель, гопкалит. Скорость реакции гетерогенного окисления оксида азота в 1,5-2,5 раза
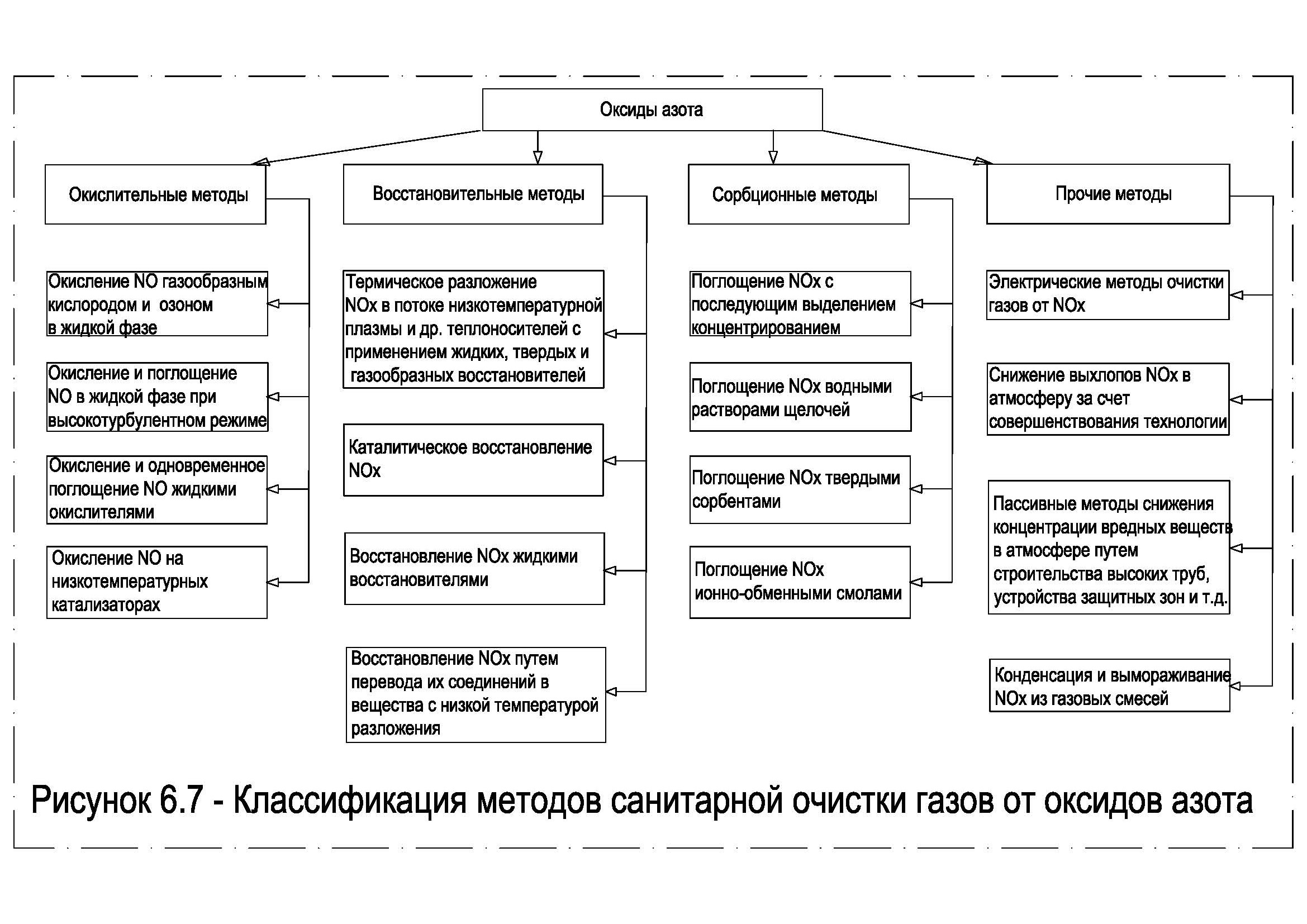
Рисунок 6.7 – Классификация методов санитарной очистки газов от оксидов азота
увеличивается. Каталитическая активность начинает проявляться при температуре 20 °С и достигает максимума при 120 °С.
Каталитическое восстановление оксидов азота. Восстановительные методы санитарной очистки газов основаны на восстановлении NOx до нейтральных продуктов в присутствии катализаторов или без катализаторов под действием высоких температур в присутствии твердых, жидких или газообразных восстановителей. Полное разложение NO2 на NO и О2 наступает при температуре около 600 °С, плное разложеие NO на элементы наступает при температурах 6000-10000 °С, основная часть NOx разлагается при температурах 1500-2000 °С. Для обезвреживания отходящих газов от NOx применяются следующие методы каталитического восстановления:
– высокотемпературное каталитическое разложение;
– селективное каталитическое восстановление;
– разложение гетерогенными восстановителями.
Высокотемпературное каталитическое восстановление. Наиболее эффективным способом обезвреживания нитрозных газов является каталитическое восстановление NOx. Процесс восстановления NOx протекает на поверхности катализаторов в присутствии газа-восстановителя[3, с. 56]. Эффективность процесса каталитического восстановления NOx определяется активностью используемого катализатора. Высокой каталитической активностью обладают катализаторы на основе платины, родия и палладия, менее активны дешевые сплавы, содержащие никель, хром, медь, цинк, ванадий, цезий и др.
Восстановителями являются: оксид углерода, водород, природный газ, пары керосина, аммиак, нефтяной и коксовый газ, азото-водородная смесь. Примеси сернистых соединений отравляют катализатор.
| 4 NO + CH4 />2 N2 + CO2 + 2 H2O + Q | (6.22) |
| 2 NO2 + CH4 />N2 + CO2 + 2 H2O + Q | (6.23) |
| 2NO + 2CO />N2 + 2 CO2 + Q | (6.24) |
| 2 NO2 + 4CO />N2 + 4 CO2 + Q | (6.25) |
| 2NO + 2 H2 />N2 + 2 H2O + Q | (6.26) |
| 2 NO2 + 4 H2 />N2 + 4 H2O + Q | (6.27) |
Каталитическое восстановление NOx начинается при температуре 149 °С в случае применения водорода в качестве восстановителя, 250 °С – при использовании СО, 339 °С – при использовании метана, 350-450 °С – при использовании природного газа. Выбрасываемые в атмосферу газы имеют обычно температуру 30-35 °С, требуют предварительного подогрева. Подогрев и восстановление NOx происходит путем смешения очищаемых газов с газом-восстановителем и сжиганием полученной смеси над слоем катализатора. Температура в зоне разложения NOx резко увеличивается. Обычно поддерживают температуру порядка 800-900 °С. Температура лимитируется термостойкостью катализатора. Допускаемое сдержание кислорода в газовой смеси: для водорода – 4,4 %, метана – 3,2 %. Прирост температуры на каждый процент вступившего в реакцию кислорода составляет: 130-140 °С для метана, 149 °С для водорода. Используется рекуперация тепла в котле-утилизаторе или газовой турбине.
Экономическая целесообразность процесса каталитического восстановления NOx в основном зависит от природы применяемого газа-восстановителя. Предпочтительно использовать водород, т.к. он дает более низкую первоначальную температуру и более полное восстановление NOx. На практике выгоднее использовать природный газ из-за дешевизны и доступности. Недостатком природного газа является повышенная температура начала реакции (350-450 °С) и высокое содержание СО в отходящих газах.
Для этого способа очистки также имеет большое значение выбор носителя катализатора, который определяет механическую прочность, термостойкость, гидравлическое сопротивление, активность катализатора, технологические параметры и его технологичность.
Катализаторы с носителями в виде насыпных шариков из оксида алюминия, керамических шариков работают 1-5 лет. Объемная скорость процесса – 3-6 тыс.ч -1 ; при начальной концентрации NOx0,3-0,5 % остаточное содержание составляет 5-10 -3 , 5-10 -4 , 10 -4 % в зависимости от газа-носителя.
Импортные катализаторы с носителями в виде гофрированных лент из хромоникелевого сплава (80 % Niи 20 % Cr) с нанесением на них платины допускают объемную скорость до 120 тыс.ч -1 , имеют высокую теплопроводность и небольшой удельный вес.
Метод восстановительной каталитической очистки газов от NOx под давлением 1-8 атм широко используется за рубежом. Аппараты выполнены различной конструкции в зависимости от заданных температур, содержания кислорода и оксидов азота в очищаемом газе, вида топлива.
В нашей стране применение каталитического метода восстановления NOx осуществляется в основном в технологии получения азотной кислоты на отечественных насыпных катализаторах АПК-2. Первая установка была запущена в 1960 г на Кемеровском азотно-туковом заводе. Газ, нагретый до 3 °С, из цехового коллектора хвостовых газов проходит в подогреватель хвостовых газов, где за счет рекуперации тепла отходящих газов нагревается до 360-420 °С, смешивается с очищаемым газом и поступает в реактор. В реакторе установлена корзина с катализатором. Температура газовой смеси за счет тепла реакции повышается до 800 °С. После реактора газ содержит 0,005 % оксида азота и 0,2-0,5 % оксида углерода. Далее газ поступает на очистку от СО.
К недостаткам метода следует отнести высокую стоимость и дефицитность используемых катализаторов; ограничения по содержанию в отходящих газах NOx (не более 0,5 %), кислорода (не более 4-5 %), соединений серы (не должны присутствовать).
Селективное каталитическое восстановление.Этот процесс выгодно отличается от высокотемпературного тем, что протекает избирательно: используемый восстановитель (аммиак) реагирует преимущественно с NOx и почти не взаимодействует с находящимися в нитрозных газах кислородом, в связи с чем его расходуют в количествах, эквивалентных содержанию в обеззараживаемых газах оксидов азота или превышающих стехиометрию на 10-50 % с целью более полного протекания следующих экзотермических реакций:
| 6NO + 4 NH3 5 N2 + 6 H2O | (6.28) |
| 6 NO2 + 8 NH3 7 N2 + 12 H2O | (6.29) |
| 8NO + 2 NH3 5 N2O + 3 H2O | (6.30) |
| 5 NO2 + 2 NH3 7 NO + 3 H2O | (6.31) |
Безвредные продукты реакции (азот и вода) являются еще одним выгодным отличием этого метода. Присутствие кислорода в отходящих газах благоприятствует реализации каталитического восстановления, реакции ускоряются, и процесс идет следующим образом:
| 4NO + 4 NH3 + O2 4 N2 + 6 H2O | (6.32) |
Селективное каталитическое восставновление происходит при низких температурах (180-360 °С) с выделением небольшого количества тепла. Температура очищаемых газов увеличивается в зоне катализа на 10-20 °С. При избытке аммиака его основное количество окисляется присутствующим в нитрозных газах кислородом по экзотермической реакции:
| 4 NH3 + 3 O2 2N2 + 6 H2O | (6.33) |
Процесс достаточно прост по аппаратурному оформлению и внедрен в производствах азотной кислоты под давлением 0,35 МПа. Отходящие нитрозные газы таких производств содержат до 0,2 % (об.) NO + NO2. Технологическая схема процесса представлена на рисунке 6.8.
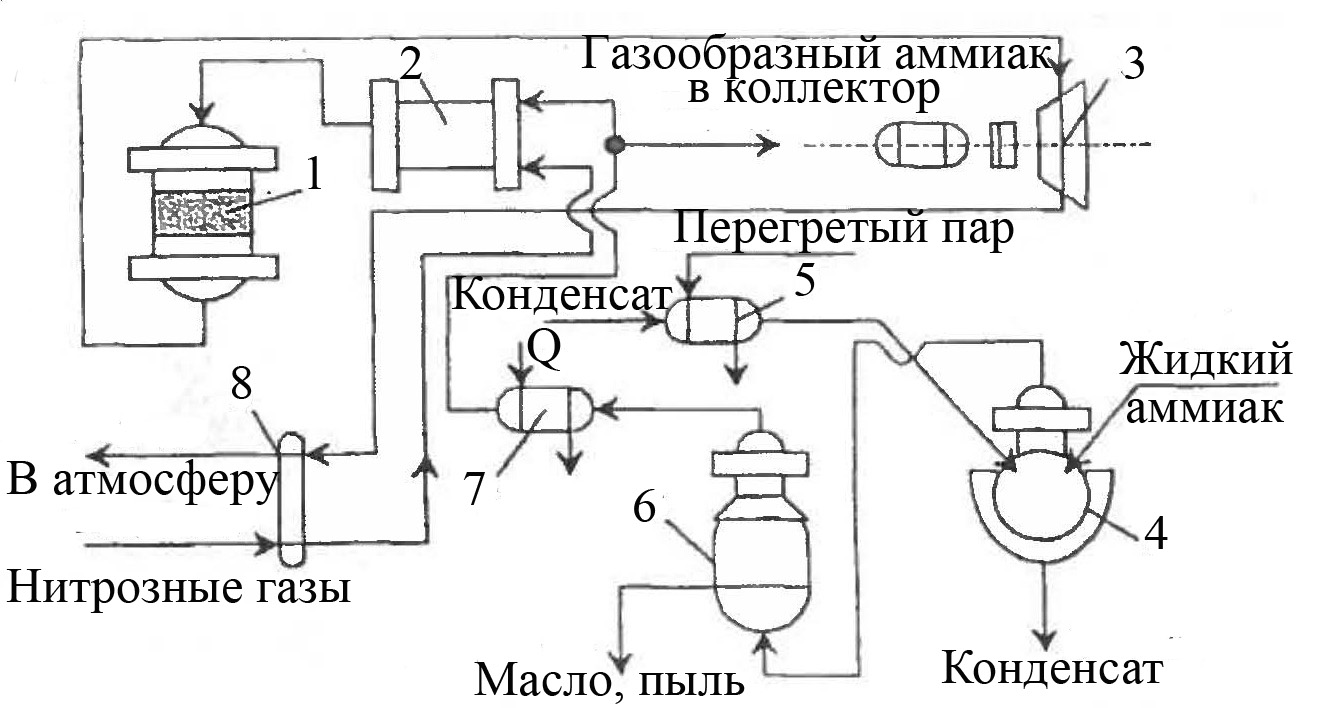
1 – реактор; 2 – смеситель; 3 – рекуперационная турбина; 4 – испаритель; 5, 7, 8 – подогреватели; 6 – фильтр
Рисунок 6.8 – Схема установки каталитической очистки отходящих нитрозных газов производств азотной кислоты под давлением 0,35 МПа
Нитрозные газы при 20-30 °С подают в подогреватель, где их нагревают до 240-280 °С и направляют в смеситель. Подаваемый в установку жидкий аммиак испаряют нагретым конденсатом. Образующиеся пары аммиака при давлении 3,5-10,0 Па очищают в фильтре, нагревают до 120 °С и смешивают с нагретыми нитрозными газами, регулируя соотношение NH3 : NOx на уровне (1,2-1,3):1. Полученную смесь направляют в реактор, где на алюмо-ванадиевом катализаторе АВК-10 идет восстановление оксидов азота аммиаком. Обезвреженные нитрозные газы при 300 °С из реактора подают на рекуперационную
турбину, откуда их направляют в подогреватель, после которого при 150-170 °С выбрасывают в атмосферу. При возможном образовании в системе аммонийных солей предусматривают периодическую остановку и пропаривание турбины насыщенным паром низкого давления.
Процесс обеспечивает обезвреживание нитрозных газов на 96 %. Содержание суммы NOи NO2 в обеззараженных газах не превышает 0,01 % (об.), NH3 – до 0,015 % (об.).
В качестве эффективных катализаторов при восстановлении нитрозных газов (содержащих 1-30 %NOх) аммиаком могут быть использованы цеолиты. Адсорбция на них NH3и NOx ускоряет их взаимодействие, обеспечивая при 330-480 °С высокую эффективность процесса обезвреживания оксидов азота.
Процесс очистки газов, при котором NOxпревращается в элементарный азот посредством введения аммиака, получил широкое распространение. Как пример можно привести технологию DENOXдатской фирмы «HALDORTOPSOEA/S». Процесс используется для очистки отходящих нитрозных газов тепловых электростанций и котельных, химических предприятий, мусоросжигательных заводов, газовых турбин, дизельных моторов и генераторов.
Наилучшим образом процесс DENOX зарекомендовал себя для очистки дымовых газов тепловых (мазутных) электростанций, где, как известно, имеют место значительные выбросы сажи.
Катализатор сотовый, тспользуемый в процессе, не забивается пылью, имеет низкое аэродинамическое сопротивление, срок службы катализатора до дезактивации – 4-5 лет, верхний слой катализатора меняется через 10 лет. Катализатор обеспечивает восстановление 90 %NOx в диапазоне температур 320-340 °С при объеме газа от 10 до 800 тыс.нм 3 /ч, концентрации оксидов азота в газе 0,04-0,09 %.
Принципиальная технологическая схема процесса DENOX представлена на рисунке 6.9.Жидкий аммиак из резервуара (3) подается в испаритель (4), откуда пары аммиака, смешиваясь с воздухом высокого (3-5 бар) давления, поступают в поток очищаемого газа через сопловый смеситель (2), обеспечивающий равномерное распределение аммиака в сечении газового потока, и далее – в реактор. Реактор имеет прямоугольное сечение, содержит 2 или более слоев катализатора, между которыми при необходимости располагают пароструйные воздуходувки (5) для улавливания пыли и летучей золы с поверхности катализатора. Внешний вид установки DENOX-процесса датской фирмы «HALDORTOPSOEA/S» представлен на рисунке 6.10.
Таким образом, процессы селективного каталитического восстановления оксидов азота используют для обработки нитрозных газов, содержащих пыль, сажу, диоксид серы и могут применять для очистки газовых выбросов в черной металлургии.
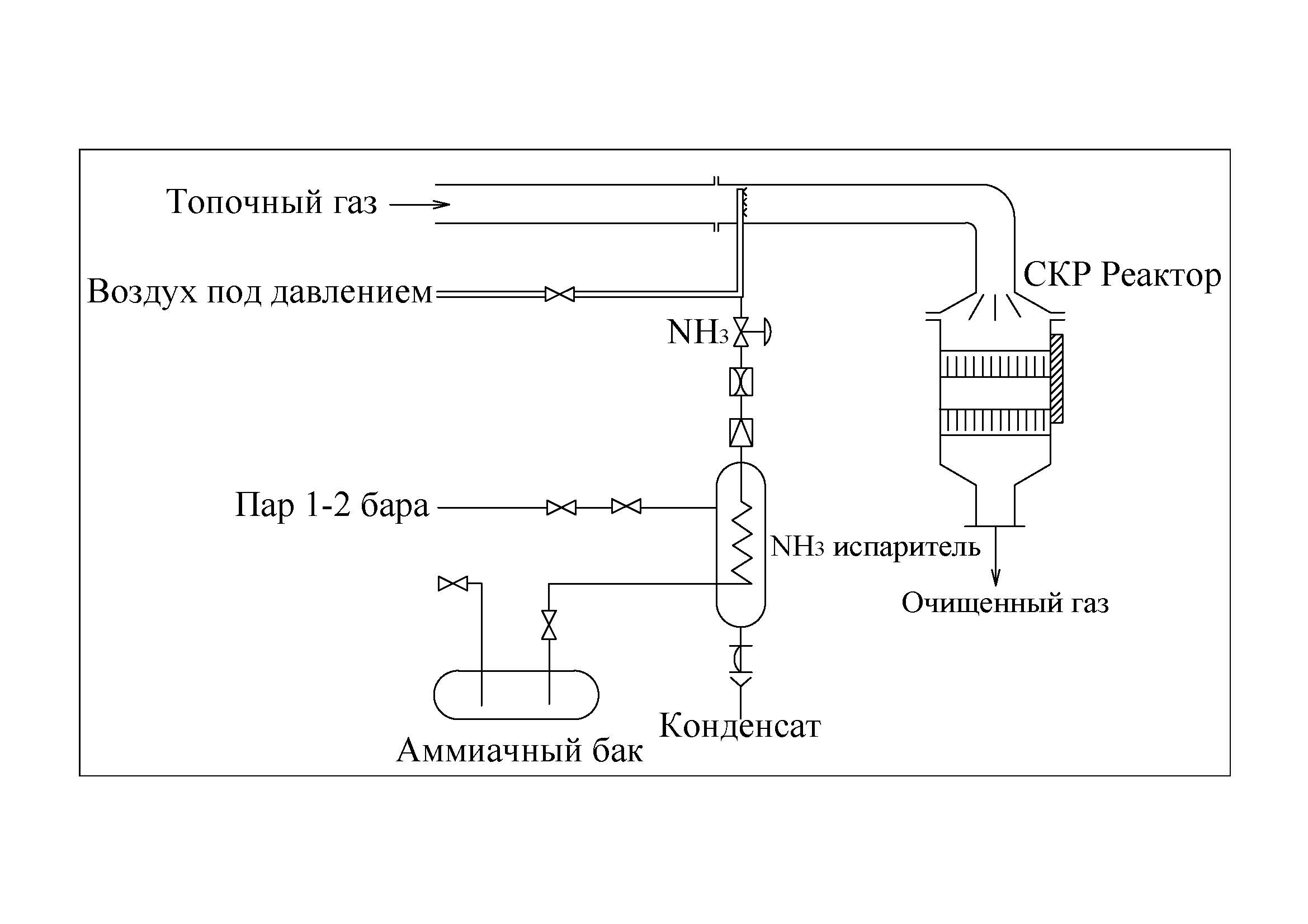
1 – реактор; 2 – смеситель; 3 – емкость аммиака; 4 – испаритель аммиака; 5 – пароструйные воздуходувки
Рисунок 6.9 – Схема установки каталитической очистки топочных газов в процессе ДЕНОКС

Рисунок 6.10 – Внешний вид установки ДЕНОКС
Разложение оксидов азота гетерогенным восстановлением.При высоких температурах (500-1300 °С) разложение азота в отходящих газах может быть проведено на твердых углеродсодержащих материалах: угле, коксе, графите. В таких процессах углерод выполняет функции как катализатора, так и топлива. Каталитическое действие углерода связано с образованием комплексов углерод-кислород:
| С + NO />(C-O) + ½ N2 | (6.34) |
| (C-O)NO />CO2 + ½ N2 | (6.35) |
Имеет место быстрая потеря активности таких катализаторов. С целью увеличения активности катализаторов и степени разложения NOx вводят в углеродистый материал карбонат натрия. С увеличением температуры скорость процесса восстановления возрастает: при 800 °С степень восстановления NOx на коксе достигает 96 %; при 1000 °С – 100 %. Высокие температуры отрицательно сказываются на технико-экономических показателях процесса.
Хемосорбционные методы часто применяются для совместной очистки газов от SO2 и NOx, что является их преимуществом. Недостаток – дороговизна применяемых сорбентов. При применении относительно дешевых сорбентов (БПК из углей канско-ачинского бассейна, коксолигнин) данные методы вполне перспективны для очистки дымовых газов.
Мокрые абсорбционные методы очистки газов от оксидов азота применяются сравнительно редко, хотя их преимуществом является довольно высокая эффективность (до 90-97 %) и рекуперативность (в отличие от каталитических). Для успешного поглощения растворителем NO должен быть окислен до NO2 с использованием активных окислителей (озон, H2O2, KMnO4, KBrO3, K2Cr2O7и др.).
| NO + H2O2 />NO2 + H2O | (6.36) |
| 3 NO2+ H2O />2 HNO3 + NO | (6.37) |
| 2 NO2 + Na2CO3 NaNO3 + NaNO2 + CO2 | (6.38) |
Представляют интерес селективные жидкие сорбенты NOx, в частности раствор FeSO4 (в качестве такого раствора могут быть использованы отработанные травильные растворы метизного производства).
Более перспективно применение хемосорбционных и каталитических процессов совместной очистки газов от SO2и NOx. В последнее время прошли промышленную проверку и считаются наиболее перспективными методы совместного окисления SO2и NOx, инициированного излучением высоких энергий или сильными окислителями (электронно-лучевой и озонный методы). Основное их преимущество – рекуперативность (получение на основе SO2и NOx ценных побочных продуктов – сульфата, нитрата аммония и др.).
Из твердых хемосорбентов HF эффективны известняк, фторид натрия, ионообменные материалы и т.д. Наиболее перспективно применение для поглощения HF глинозема с последующим его использованием в самом алюминиевом производстве. Для этих целей используются как аппараты с псевдоожиженным слоем Al2O3, так и рукавные фильтры с нанесенным слоем глинозема.
Отходящие газы, содержащие одновременно Cl2 и HCl, подвергаются мокрой очистки очистке в скрубберах(1-я ступень – очистка водой с получением 10-18 %-ной HCl, а 2-я ступень – очистка от Cl2 при помощи известкового молока). Более эффективно применение для поглощения Cl2Na2CO3, а также CCl4, TiCl4. Из твердых сорбентов Cl2 хорошо себя зарекомендовал лигнин и лигносульфонат Ca (отходы лесохимии). Для поглощения HCl используются сульфаты и фосфаты Cu, цеолиты и некоторые промышленные отходы (доменные и сталеплавильные шлаки и шламы, оксиды щелочных и щелочноземельных металлов и др.).
Каталитическая очистка газовых выбросов: методы и технологии

Каталитическая очистка газовых выбросов, неизбежно сопровождающих многие производственные процессы, является одним наиболее эффективных методов химического обезвреживания содержащихся в них вредных веществ. Суть каталитических методов очистки газовых выбросов заключается в реализации химических взаимодействий, приводящих к конверсии подлежащих обезвреживанию вредных веществ в другие, без- или маловредные, в присутствии специальных катализаторов.
К числу загрязняющих атмосферный воздух вредных веществ относятся не только многочисленные летучие органические соединения (ЛОС) образующиеся в процессе функционирования различных промышленных производств, например, химических и нефтехимических, но и дурнопахнущие, выделяемые, например городскими очистными сооружениями, а также загрязняющие вещества, входящие в состав газовых выбросов, производимых промышленным оборудованием, работающим на двигателях внутреннего сгорания.
На законодательном уровне утверждены нормы, призванные обеспечить уменьшение выбросов вредных веществ в атмосферный воздух.
Решения для промышленности: каталитические методы очистки газовых выбросов
Известно несколько разновидностей каталитических методов очистки, отличающихся по механизму, природе используемых катализаторов и применяемых в зависимости от типа преобладающего вредного вещества в газовых выбросах производства: пиролюзитный, озонокаталитический, жидкостно-контактный и радикально-каталитический.
Для снижения выбросов в атмосферу вредных веществ, содержащихся в промышленных выбросах, например, металлургических производств, а это в основном NOx, могут быть использованы как первичные, так и вторичные меры.
Первичные меры направлены на предотвращение образования вредных веществ на этапе подготовки производства (использование новых современных технологий, переход на альтернативные расходные материалы и энергоносители), они достаточно эффективны, но весьма затратны.
Вторичные меры включает удаление вредных веществ путем очистки газовых выбросов, образующихся на различных стадиях производства. Использование этих мер не требует каких-либо структурных изменений и не влияет на ход принятого технологического процесса производства продукции.
При выборе подходящих мер, как правило обращают внимание на экологический и экономический аспект, то есть, будут ли инвестиционные затраты, связанные с сокращением выбросов вредных веществ, адекватны прибыли от производства. На рынке представлен широкий спектр оборудования, реализующего различные методы каталитической очистки газовых выбросов, которые позволяют эффективно уменьшить концентрацию выбрасываемых вредных веществ.
В зависимости от объема производства и финансовых возможностей компании предприниматель должен решить, может ли он использовать вторичные меры – каталитические методы очистки газовых выбросов, или использовать первичные меры, при которых он будет использовать возобновляемые энергоресурсы и не столкнется с проблемой управления отходами.
Для минимизации концентрации вредных веществ в газовых выбросах могут быть использованы различные химические реакции, такие как абсорбция и адсорбция, а также каталитическое восстановление и каталитическое окисление.
Промышленные каталитические нейтрализаторы
Каталитический нейтрализатор, представляющий собой систему очистки отработавших газов, установленный на генераторной станции, специальной технике обеспечивает степень очистки отработавших газов ДВС:
- по оксиду углерода (CO) – 90-97%;
- по углеводородам (CH) – 85-95%;
- по оксидам азота (NOx) – 65-95%;
- по содержанию твердых частиц (саже, РМ) – 85-95%.
Система очистки отработавших (выхлопных) газов может состоять из трех последовательных ступеней, в зависимости от требований производства:
Сажевый фильтр.
Мелкие частицы сажи, образующиеся в двигателе внутреннего сгорания, могут оказывать канцерогенное действие, если они прикрепляются к легочной ткани. Волокнистый сажевый фильтр может фильтровать мелкие частицы отработавших газов. Частицы сгорают при рабочей температуре внутри системы на пропитанной катализатором поверхности волокна.
Сажа, осаждаемая на фильтре, состоит в основном из частиц углерода (C) и углеводородов. Существует два основных метода удаления частиц:
1. сгорание с кислородом (O2): [C] + O2 → CO 2 2. сгорание с диоксидом азота (NO2): [C] + NO2 → CO2 + NO
Характеристики двух разных методов отражены в таблице:

Регенерация на основе O2 Регенерация на основе NO2 Температура, необходимая для регенерации Требуется температура около 600 °C (или 400 °C с топливным катализатором). Реакция происходит от 250 °С. Используемый газ O2 в потоке выхлопных газов. NO2 должен быть воспроизведен из NO в потоке выхлопных газов.
Оборудование для селективного каталитического восстановления оксидов азота (NOx).
Этот процесс используется для уменьшения оксидов азота, образующихся во время процесса сгорания углеводородного топлива, сопровождающегося выделением энергии. NO (оксид азота) представляет собой бесцветный газ, который окисляется в воздухе с образованием NO2 (диоксид азота). В высоких концентратах он вызывает симптомы паралича нервной системы. NO2 - красно-коричневый газ с резким запахом. Под воздействием солнечного света и углеводородами, образует смог. Оксиды азота восстанавливаются в кислородсодержащих выхлопных газах с помощью процесса SCR (Selective Catalytic Reduction, селективное/выборочное каталитическое восстановление). Отработавший газ, обработанный дозированным реагентом мочевины, проходит через тонкостенные сотовые преобразователи, восстанавливая оксиды до воды и азота. Процесс с мочевиной – выгодная альтернатива аммиаку в качестве реагента для снижения уровня отравляющих веществ в выхлопных газах двигателя. По сравнению с аналогом реагент обладает значительными преимуществами в отношении транспортировки, хранения и обработки, при этом она значительно дешевле.
Оборудование для каталитического окисления СО и несгоревших углеводородов.
Этот процесс используется для снижения уровня окиси углерода и несгоревших углеводородов в выхлопных газах. Это достигается путем каталитического окисления. Такой катализатор может быть установлен после стадии SCR. Несгоревшие углеводороды могут быть обнаружены в выхлопных газах двигателей внутреннего сгорания. Такие выхлопные газы содержат различные вещества с различными свойствами:
Насыщенные углеводороды (парафины) практически не имеют запаха и могут оказывать слабое наркотическое действие.
Ненасыщенные углеводороды (олефины, ацетилены) – одна из составляющих городского смога.
Ароматические углеводороды представляют собой нервно-паралитические яды с наркотическим эффектом, а некоторые служат канцерогенными альдегидами с резким запахом и даже в низких концентрациях сильно раздражают слизистые глаз и носа.
Системы очистки выхлопных газов могут быть установлены как на стационарном, так и на мобильном оборудовании на первичных двигателях внутреннего сгорания, работающих на газе и жидком топливе.

Реверсивный метод каталитической очистки газа
Среди каталитического дожигания можно выделить реверсивный метод каталитической очистки газа, который благодаря низкому энергопотреблению особенно подходит для очистки газов от органических загрязнителей, выбрасываемых промышленностью в атмосферу. Установки обратного типа изготавливаются в соответствии с типовой серией с диапазоном производительности от 300 до 15 000 м3/ч для концентраций органических соединений от нескольких сотен мг до нескольких грамм на м3.
Эффективность очистки зависит от типа загрязнения и составляет до 98%. При концентрациях органических соединений выше 0,7 г/м3 установка работает автотермически (без затрат энергии для нагрева реактора). Побочные продукты – азот и вода нейтральны для окружающей среды. Способ более экономичен, чем термическое сгорание, так как работает при более низких температурах. Недостаток – высокие затраты на внедрения по причине стоимости каталитически активных металлов.
Особенности эксплуатации каталитических нейтрализаторов
Каталитический нейтрализатор использует каталитическое химическое преобразование для преобразования оксида углерода (CO) и несгоревших углеводородов (CH) в нетоксичный диоксид углерода и воду. Это преобразование осуществляется на металлической сотовой подложке, покрытой активным каталитическим материалом. Катализатор способен обеспечить степень очистки загрязняющих веществ – до 90% при оптимальной рабочей температуре от 250°C.
- Сфера применения.
Катализатор подходит для любых дизельных двигателей, использующихся на такой технике, как генераторные агрегаты с первичной мощностью или резервные генераторы, землеройное и погрузочно-разгрузочное оборудование (спецтехника, погрузчики). В частности, катализаторные установки применяют для оснащения техники, используемой в ограниченном пространстве, таком как туннели, склады и шахты. - Установка.
Важно монтировать узел как можно ближе к выпускному коллектору двигателя. Для обеспечения максимальной каталитической эффективности катализатора требуется достаточно высокая температура. - Срок эксплуатации.
В основе работы каталитического нейтрализатора лежит осуществление каталитической реакции, следовательно, срок службы катализатора теоретически не ограничен. Узел может выйти из строя в результате ошибок при эксплуатации (повышенная вибрация двигателя, погрешности монтажа, абразивное воздействие выхлопных газов).
Решения от ЭКОЭНЕРГОТЕХ
Компания «ЭКОЭНЕРГОТЕХ» стремится привлечь внимание к проблеме попадания в атмосферу в составе промышленных газов вредных веществ, таких как угарный газ, NOx, SOx, твердые частицы и углеводороды. В соответствии с требованиями законодательства владельцы предприятий будут вынуждены применять решения для сокращения выбросов. Это могут быть операции, как конструктивного характера, так и внедрение методов каталитической очистки. В каталоге предприятия вы найдете проекты различных установок позволяющих добиться снижения выбросов токсичных соединений и СО2 и адаптироваться к требованиям действующих экологических норм и условий. Мы поможем вам внедрить на производстве очистные системы в соответствии с представленными требованиями.
Разработка блочного катализатора сотовой структуры и реактора очистки выхлопных газов от оксидов азота Текст научной статьи по специальности «Химические технологии»
Аннотация научной статьи по химическим технологиям, автор научной работы — Векшин В.А., Грабовецкая Е.Р., Лобойко В.А., Кобзев А.В.
Производство азотной кислоты связано с выбросами в атмосферу газов, содержащих токсичные оксиды азота . При окислении аммиака образуется оксид азота (II), который затем окисляется кислородом воздуха до оксида азота (IV), и, в результате неполноты его поглоще¬ния в абсорбционных колоннах, вместе с недоокисленным NO, выбрасывается в атмосферу. Без соответствующей очистки содержание NO + NO2 (NOx) в отходящих газах после абсорб¬ции может достигать 0,15 % об. Как результат, в районах расположения химических пред¬приятий может наблюдаться довольно высокий уровень локального загрязнения атмосферы этими оксидами. Данная проблема заставляет исследователей искать пути снижения вредно¬го влияния данных соединений на окружающую среду и живые организмы. Использование каталитического обезвреживания позволяет существенно снизить количество оксидов азота , которые выбрасываются промышленными предприятиями. Важным направлением в реше¬нии представленной задачи является разработка высоко-эффективных катализаторов очистки отходящих газов. Данные способы очистки известны достаточно давно. Восстановителями могут служить метан, водород, СО и др., но более перспективным направлением совершен¬ствования рассматриваемого процесса является применение в качестве восстановителя амми¬ака, поскольку его расход в этом случае незначителен. В отличие от других восстановителей он селективно реагирует с оксидами азота , позволяет существенно снизить температуру про¬цесса и отказаться от использования дорогостоящих и дефицитных восстановителей.
Похожие темы научных работ по химическим технологиям , автор научной работы — Векшин В.А., Грабовецкая Е.Р., Лобойко В.А., Кобзев А.В.
Текст научной работы на тему «Разработка блочного катализатора сотовой структуры и реактора очистки выхлопных газов от оксидов азота»
Векшин В.А., н. с., Грабовецкая Е.Р., канд. биолог. наук, доц.
Харьковский национальный медицинский университет Лобойко В.А., канд. техн. наук, доц., Кобзев А.В., канд. техн. наук, доц.
Национальный технический университет «Харьковский политехнический институт»
РАЗРАБОТКА БЛОЧНОГО КАТАЛИЗАТОРА СОТОВОЙ СТРУКТУРЫ И РЕАКТОРА ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ОТ ОКСИДОВ АЗОТА
Ключевые слова: оксиды азота, очистка, кинетика, катализатор, реактор._
Введение. В настоящее время для очистки отходящих газов от оксидов азота на азотно-кислотных предприятиях используют каталитическое восстановление с применением алюмо-ванадиевых катализаторов типа АВК-10 и их модифицированных аналогов. Основным недостатком таких контактов является высокое гидравлическое сопротивление, что не позволяет использовать их в процессах с высокими объемными скоростями. В последние годы большой интерес вызывает разработка блочных катализаторов сотовой структуры, которые лишены указанных недостатков [1]. Преимущества таких катализаторов заключается в том, что при высокой скорости подачи газа, они обеспечивают низкий перепад давления до и после каталитической системы. При этом металлические блоки проще керамических в изготовлении, имеют высокую механическую прочность, теплопроводность и устойчивость к перепадам температуры. Применение металлических блочных катализаторов позволяет достигать времени контактирования на уровне нескольких милли-
секунд, а простота загрузки и отсутствие пыли явно свидетельствует о том, что блочные катализаторы являются более перспективными, чем те, которые применяются сегодня в промышленности [2]. На кафедре технологии неорганических веществ, катализа и экологии НТУ «ХПИ» был разработан катализатор очистки отходящих газов от оксидов азота основанный на титановом носителе, покрытый оксидным слоем ТЮ2 с последующей, пропиткой раствором гексахлороплатиновой кислоты Н2Р1С16 и модифицированием одноосновными органическими кислотами [3]. Данный катализатор показал высокую активность как в лабораторных условиях, так и в процессе промышленных испытаний на ЧАО «Северодонецкое объединение «Азот». Это позволило продолжить исследования в данном направлении, где следующим шагом являлась разработка промышленного каталитического блока и самого реактора очистки.
Методология. Активность катализатора определяли на лабораторной установке проточного типа, с помощью объемного анализа мето-
дом эвакуированных колб. Математическую обработку осуществляли методом регрессионного анализа с применением программного обеспечения Microsoft Excel 2003 и Statgraphics Centurion XV.
Основная часть. Одним из основных этапов разработки каталитического реактора являлось определение кинетических закономерностей химических превращений, которые происходят на конкретном катализаторе. Для этого были проведены лабораторные исследования на установке проточного типа с реактором из кварцевого стекла при технологических параметрах, максимально приближенных к производственным: концентрация оксидов азота в газовой смеси: Cnox= 0,12 - 0,16 % об. (Cno : Cno2= 50 : 50); концентрация восстановителя (аммиака): Cnh3= 0,13 . 0,22 % об.; газ-носитель - воздух;
температурный интервал: 423. 573 К; объемная скорость газовой смеси 5000 . 15000 ч-1. Расчет критерия Рейнольдса показал, что для данных условий характерен ламинарный режим движения газового потока ^е > 710), а процесс восстановления оксидов азота протекает в области внешней диффузии, что по данным авторов [4] вполне характерно для катализаторов данного типа. Время контактирования на катализаторе рассчитывали по формуле: Уд ■ ц
где Ур - объем зоны реакции, м3;Уг - расход газа, м3/ч; ц - доля свободного объема катализатора (принимали 0,5).
Результаты расчетов приведены в табл. 1.
Зависимость времени контактирования от объемной скорости
Объемная скорость, ч 1 5000 10000 15000
Время контактирования, т, с 0,36 0,18 0,12
При расчете константы скорости пользовались выкладками, что кинетику реакций восстановления оксидов азота с помощью аммиака можно рассчитать согласно уравнения первого порядка по оксидам азота и нулевого порядка по аммиаку, при его избытке [5]. В данном случае ввиду высокой вероятности протекания побочных реакций окисления аммиака, экспериментальную (кажущуюся) константу скорости рассчитывали по уравнению первого порядка, согласно определенным в лабораторных условиях
и усредненным концентрациям NOx:
где - начальная концентрация оксидов азо-
та, %, об; Йем0 - конечная концентрация оксидов азота, %, об; т - время контактирования, с. Результаты расчетов приведены в табл. 2.
Зависимость кажущейся константы скорости от температуры и объемной скорости
5000 10000 15000
423 11,373 12,050 11,552
473 19,695 22,442 21,586
523 24,165 25,826 24,297
Основываясь на данных представленной выше таблицы рассчитывали истинную константу скорости, которую находили методом линеаризации функции кэкс.= /(Г) с последующим определением предэкспоненциального множителя ко и энергии активации Еа. Учитывая, что при всех объемных скоростях зависимость кэкс. от температуры экспоненциальная, линеаризацию осуществляли путем создания обратной функции 1пкекс.= /(1/Г). Расчеты проводили
методом регрессионного анализа в StatgrapЫcs
Centurion XV. Также, для выявления возможного влияния побочных реакций на стадии каталитического восстановления, были проведены расчеты констант скорости процесса окисления аммиака. За основу были приняты усредненные экспериментальные данные «холостых» экспериментов, без оксидов азота, при аналогичных условиях. Дальнейшая обработка полученных данных позволила определить скорость основных и побочных реакций. Эти результаты представлены в табл. 3.
Константа скорости и скорость реакций (-ёе/ёт) восстановления NOx и окисления NH3 в зависимости от температуры процесса и начальной концентрации (С) при объемной скорости
газового потока 10000 ч-1
Температура, К Восстановление N0% Окисление ^ЫН3
N , МОх(л) % об. к, с-1 -ёе/ёт, % об./с NNH■5(и), % об. к, с-1 -ёе/ёт, % об./с
423 0,14 12,791 1,789 0,15 2,11 0,320
473 0,14 19,647 2,783 0,14 4,48 0,588
523 0,13 27,801 4,332 0,14 8,22 1,242
Данные таблицы показывают, что в данном температурном интервале скорость реакций восстановления оксидов азота намного превышает скорость возможных побочных реакций окисления аммиака. После преобразования объемной
концентрации в молярную, методом регрессионного анализа была построена кинетическая модель процесса восстановления NOx с помощью аммиака:
Проверка модели показала отклонение от экспериментальных данных не более ± 0,01 %.
Полученные результаты дали возможность перейти к прикладным исследованиям по разработке каталитического блока сотовой структуры и промышленного реактора к нему.
Промышленный реактор очистки рассчитывали, опираясь на данные лабораторных ис-
следований, но расчеты проводили принимая расход отходящих газов в условиях производства НК03 - 50 000 м3/ч. Линейную скорость определяли исходя из данных лабораторных исследований, объем реактора и площадь его поперечного сечения находили опираясь на промышленный расход газа (« 14 м3/с). Результаты расчетов приведены в табл. 4.
Объемная скорость, ч-1 Время контактирования, т, c Расход газа Кг, м3/с Объем реактора Vp, м3 Линейная скорость w, м/с Площадь поперечного 2 сечения реактора, ¥, м2
15000 0,12 14 3,36 4,38 3,2
10000 0,18 14 5,04 2,81 4,98
5000 0,36 14 10,08 1,35 10,34
На основе представленных выше данных была сформирована общая конструкция ката-лизаторного блока, который представляет собой гофрированные, оксидированные и модифицированные одноосновными органическими кислотами титановые пластины, на которые нанесен слой каталитически активного вещества. Пластины собраны так, чтобы вершины гофр соприкасались, образуя каналы квадратного сечения [6]. В местах, где гофры прикасаются одна к другой, пластины закрепляются точечной сваркой, образуя единый катализаторный блок.
Для расчета размера катализаторной ячейки использовали выкладки авторов [7], согласно которым определяли пограничный слой:
Расчеты показали, что для достижения полноты очистки необходимо и достаточно сформировать блок с ячейками квадратного сечения размером 6 х 6 мм. Для определения длины блока использовали выражение (5), приведенное авторами [8].
где а - расход газа, м/с, х - степень восстановления NOx, д.ед.
После интегрирования выражение (5) имеет
Данное уравнение было решено с учетом привязки площади поверхности к количеству стенок ячеек (пластин):
где к - константа скорости, приведенная к единице поверхности, м2/с, I - длина пластины, м, ¥ - площадь удельной поверхности, м2/г, п - количество пластин, шт.
С помощью приведенной формулы определяли два параметра: длину ячеек I и их количество п.
Опираясь на полученные данные был проведен полный расчет реактора очистки, при осуществлении которого также учитывалось,
что данный аппарат будет эксплуатироваться в условиях производства и его параметры должны быть жестко привязаны к требованиям, которые предъявляются промышленным реакторам.
Размеры реактора определяли так, чтобы он мог обеспечивать эффективное восстановление оксидов азота до необходимых санитарных норм в промышленных условиях при расходе газовых выбросов порядка 50 000 м3/ч. Расчеты показали, что оптимальными размерами реактора будут: диаметр 0 = 2 м; высота Н = 1,6 м.
Конструктивно реактор состоит из корпуса в виде цилиндрической обечайки 1, с двух сторон которой расположены конические крышка 2 и днище 3. В зоне реакции установлен катализа-торный блок 4. Между корпусом и катализатор о м находится зона обогрева 5, в которую через штуцеры 6 поступает горячий пар. Внизу расположены штуцеры подачи газов: оксидов азота -7 и аммиака - 8. Газы смешиваются в объеме конического днища и поступают на блок катализатора, где протекает реакция с образованием молекулярного азота и воды, которые через штуцер 9 выбрасываются в атмосферу (рис. 1).
Рис. 1. Общий вид Гидравлическое сопротивление катализа-торного блока рассчитывали по формуле Дарси-Вейсбаха, представленной авторами [9], а сопротивление промышленного катализатора АВК-10 определяли по методике для зернистых материалов [10]. Расчеты показали, что гидравлическое сопротивление АР на метр слоя разработанного катализатора в 12 раз меньше, чем у катализатора АВК-10 в условиях промышленной очистки.
Выводы. В результате проведенных исследований были рассчитаны кинетические показатели реакций процесса очистки оксидов азота с помощью NH3 на нанесенном платиновом ка-
реактора очистки тализаторе сотовой структуры. Полученные данные показали, что в интервале температур 423. 523 К скорость реакций восстановления КОх намного превышает скорость побочных реакций окисления аммиака. Полученное кинетическое уравнение (3) дало возможность прогнозировать эффективность процесса очистки, в том числе и в условиях производства, а данные расчета константы скорости легли в основу проектирования промышленного блочного катализатора очистки отходящих газов от оксидов азота и реактора к нему. Исследования также показали, что гидравлическое сопротивление разработанного блока в 12 раз ниже, чем у промыш-
ленного гранулированного контакта АВК-10, что дает возможность снизить затраты на создание избыточного давления для продувки газа сквозь слой катализатора.
1. Тошинский В.И. Каталитические и абсорбционные процессы в технологии серной кислоты под повышенным давлением: Автореф. дис. докт. техн. наук. Харьков, 1990. 40 с.
2. Менон П.Г, Цвинкельс М.Ф.М., Иохансон Е.М., Ярее С.Г. Блочные сотовые катализаторы в промышленном катализе // Кинетика и катализ. 1998. Т.39. № 5. С. 670-681.
3. Лобойко А.Я., Векшин В.А., Маркова Н.Б., Ворожбиян М.И., Шапарева Л.П. Исследование влияния технологии приготовления катализатора на распределение каталитически активного вещества по поверхности носителя // Сучасш проблеми технологи неоргашчних речовин: збiрник наукових праць ДДТУ - Дшпродзер-жинськ.2008. № 2(10). С. 59-62.
4. Мухленов И.П., Добкина Е.И., Дерюжкина
В.И., Сороко В.Е.. Технология катализаторов. Л.: Химия, 1989. 272 с.
5. Матрос Ю.Ш., Носков А.С., Чумаченко В.А., Пармон В.Н. Каталитическое обезвреживание отходящих газов промышленных производств. Новосибирск: Наука. 1991. 221 с.
6. Патент на корисну модель UA 90106 U 12.05.2014, Лобойко О.Я, Гринь Г.1., Векшин В.О., Маркова Н.Б., Багрова 1.В, Микиша Г.В. Споаб виготовлення блочного каталiзатора очистки ви-кидних газiв вiд оксидiв ттрогену. 2014. Бюл. № 9
7. Воробьев А.Х. Диффузионные задачи в химической кинетике. Изд-во Моск. ун-та, 2003. 98 С.
8. Ветошкин А.Г. Процессы и аппараты газоочистки. Пемза: Изд-во ПГУ. 2006. 201 с.
9. Михалев М.А. Гидравлический расчет напорных трубопроводов // Инженерно-строительный журнал. 2012. № 6. С.20.
10. Товажнянский Л.Л., Готлинская А.П., Лещенко В.А., Нечипоренко И.А., Чернышов И.С. Процессы и аппараты химической технологии. Харьков: НТУ «ХПИ», 2004. 1176 с.
Vekshin V.A., Grabovetskaya E.R., Loboyko V.A., Kobzev A.V.
CREATION OF CELLULAR BLOCK CATALYST AND REACTOR FOR PURIFICATION OF EXHAUST GASES FROM NITROGEN OXIDES
Problems of environment pollution with nitrogen oxides are considered in the article. Role of catalytic purification in the process of decreases of NOx concentration in exhaust gases in nitric acid production is shown. Advantages of block metallic catalysts having cellular structure are described in comparison with industrial granulated catalysts. Based on the laboratory investigations, kinetic parameters of nitrogen oxides reduction using ammonia on the developed catalyst have been calculated. Sizes of catalytic block have been determined and reactor for catalytic purification for nitric acid production has been proposed. It is noted that created block metallic catalyst possesses low hydraulic resistance in comparison with industrial granulated catalysts. This allows reducing power expenses for overpressure. Key words: nitrogen oxides, purification, kinetics, catalyst, reactor.
Читайте также:

