Во сколько раз изменится давление газа в цилиндре
Добавил пользователь Cypher Обновлено: 05.10.2024
Тест по физике Уравнение Клапейрона-Менделеева для 10 класса
Тест по физике Уравнение Клапейрона-Менделеева. Изотопы для 10 класса с ответами. Тест включает в себя 2 варианта. В каждом варианте по 5 заданий.
1 вариант
1. Как изменится давление идеального газа при увеличении температуры и объема газа в 4 раза?
А. Увеличится в 4 раза
Б. Уменьшится в 4 раза
В. Не изменится
2. В одинаковых сосудах при одинаковой температуре находятся водород (Н2) и углекислый газ (СО2). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки сосуда?
А. Водород в 22 раза
Б. Углекислый газ в 22 раза
В. Водород в 11 раз
3. Какому процессу соответствует график, изображенный на рисунке 26?
А. Изохорному
Б. Изобарному
В. Изотермическому
4. Во сколько раз изменится давление воздуха в цилиндре (рис. 27), если поршень переместить на l/3 влево?
А. Не изменится
Б. Увеличится в 1,5 раза
В. Уменьшится в 1,5 раза
5. Во сколько раз отличается плотность метана (СН4) от плотности кислорода (O2) при одинаковых условиях?
А. Плотность метана в 2 раза меньше
Б. Плотность метана в 2 раза больше
В. Плотность газов одинакова
2 вариант
1. Как изменится давление идеального газа при уменьшении температуры и объема газа в 2 раза?
А. Увеличится в 2 раза
Б. Не изменится
В. Уменьшится в 2 раза
2. В одинаковых баллонах при одинаковой температуре находятся кислород (O2) и метан (СН4). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки баллона?
А. Кислород в 2 раза
Б. Метан в 2 раза
В. Метан в 4 раза
3. Какому процессу соответствует график, изображенный на рисунке 28?
А. Изохорному
Б. Изотермическому
В. Изобарному
4. Во сколько раз изменится давление воздуха в цилиндре (рис. 29), если поршень переместить на l/3 вправо?
А. Не изменится.
Б. Увеличится в 1,33 раза
В. Уменьшится в 1,33 раза
5. До какой температуры при нормальном давлении надо нагреть кислород, чтобы его плотность стала равна плотности азота при нормальных условиях?
А. До 39 °С
Б. До 59 °С
В. До 29 °С
Ответы на тест по физике Уравнение Клапейрона-Менделеева. Изотопы для 10 класса
1 вариант
1-В
2-А
3-А
4-Б
5-А
2 вариант
1-Б
2-Б
3-В
4-В
5-А
Во сколько раз изменится давление газа в цилиндре, если его объем.уменьшить,продвинут поршень на 1/3 высоты цилиндра? Темперарура газа не меняется.
необходимо расплавить. а) Какое количество теплоты потребуется для этого? б) Какое количество теплоты необходимо затратить для превращения льда в воду, если начальная температура льда 10 °С? в) Изобразите процесс графически, откладывая по оси абсцисс подводимое количество теплоты, а по оси ординат – температуру вещества. Какая физическая величина при плавлении вещества остается неизменной? Почему?
4 раза, а концепция - увеличилась в 8 раз.
Только с объяснениями) Срочно)
а) см3 б) л в) м3 г) дм3 д) м
2. Физическая величина, давление (p), определяется по формуле:
3. Выражение V1T2 = V2T1 (при p = const,
m = const) является:
а) законом Бойля-Мариотта
б) законом Гей-Люссака
в) законом Шарля
г) уравнением Менделеева-Клайперона
д) основным уравнением МКТ
4. При изохорном процессе в газе не изменяется (при m = const) его:
а) давление б) объем в) температура
г) средняя квадратичная скорость молекул
д) средняя кинетическая энергия молекул
5. Как изменится давление идеального газа при увеличении его объема в 2 раза и уменьшении абсолютной температуры в 2 раза?
а) уменьшится в 2 раза
б) увеличится в 2 раза
в) уменьшится в 4 раза
г) увеличится в 4 раза
6. Какой из графиков на рисунке является графиком изотермического процесса идеального газа?
7. Кислород находится в сосуде вместимостью
0,4 м3 под давлением 8,3*105 Па и при температуре 320 К. Масса газа равна:
а) 0,2 кг б) 0,4 кг в) 4 кг г) 2 кг д) 0,5 кг
8. Какова плотность воздуха (М = 29*10-3 кг/моль) в камере сгорания дизельного двигателя при температуре 503 °С, если давление воздуха равно 400 кПа?
а) 1,2 кг/м3 б) 1,5 кг/м3
в) 1,8 кг/м3 г) 2,1 кг/м3 д) 2,4 кг/м3
9. При давлении 105 Па и температуре 15 °С объем воздуха 2 л. При каком давлении воздух займет объем 4 л, если температура его станет 20 °С?
а) 103 Па б) 3,5*104 Па в) 0,5*105 Па
г) 0,8*106 Па д) 2*105 Па
10. В баллоне находится газ при t = 27 °С. Во сколько раз изменится давление газа, если 50% его выйдет из баллона, а температура при этом увеличится до 600 К?
а) увеличится в 2 раза
в) уменьшится в 2 раза
г) увеличится в 4 раза
д) уменьшится в 4 раза
11. Масса кислорода m при давлении p занимает объем V. Как изменится температура газа, если при увеличении давления до 3p его объем уменьшился до , при этом 10% газа улетучилось?
б) увеличится в 2 раза
в) уменьшится в 3 раза
г) увеличится в 4 раза
д) уменьшится в 6 раз
12. При температуре t = 36 °С и давлении
p = 0,7 МПа плотность газа ρ = 12 кг/м3. Определите молярную массу газа.
а) 8*10-3 кг/моль б) 16*10-3 кг/моль
в) 32*10-3 кг/моль г) 44*10-3 кг/моль
13. На рисунке дана изохора для 360 г водорода. Какому объему соответствует эта изохора?
14. Для того, чтобы плотность идеального газа при неизменном давлении увеличилась в 2 раза, абсолютную температуру газа следует:
а) увеличить в 2 раза
б) увеличить в 4 раза
в) увеличить в раз
г) уменьшить в 2 раза
д) уменьшить в 4 раза
15. В сосуде объемом V при давлении p и температуре Т может находиться ν молей идеального газа, равное
Во сколько раз увеличится период колебаний математического маятника,если его поднять с уровня моря на Эверест?Радиус Земли 6400 км. Высота Эвереста над уровнем моря 8,9 км.
Увеличится в 2 раза; Б. Уменьшится в 2 раза; В. Увеличится в 10 раз; Г. Не изменится.
Физика (заочники). Молекулярная физика. Состояние идеального газа.
1. Выходное отверстие велосипедного насоса диаметром d = 4 мм зажато пальцем
(см. рис.). Найти силу давления воздуха на палец в тот момент, когда поршень, сжимая
воздух, не доходит до конца насоса на расстояние l1 = 2 см. Длина насоса l = 42 см.
Процесс считать изотермическим.
2. Песок насыпают в цилиндр и плотно закрывают поршнем. При суммарном объеме песка и
воздуха Vl давление воздуха равно р1; а при суммарном объеме V2 давление воздуха равно р2. Найти
объем песка V, если температура неизменна.
3. Упругий шар, наполненный газом и имеющий радиус r1 = 10 см при внешнем давлении
р0 = 105 Па, помещен под колокол воздушного насоса. Каким должно стать внешнее давление рx, чтобы
радиус шара увеличился на Δr = 0,5 см? Давление, создаваемое оболочкой, р = аr2, где а = 1,66·107 Па/м2
и г − радиус шара. Температуру газа считать неизменной.
4. Газовый термометр состоит из шара с припаянной к нему горизонтальной
стеклянной трубкой (см. рис.). Капелька ртути, помещенная в трубку, отделяет объем
шара от внешнего пространства. Площадь поперечного сечения трубки S = 0,1 см2. При
температуре Т1 = 273 К капелька находилась на раcстоянии l1 = 30 см от поверхности
шара, при температуре Т2 = 278 К − на расстоянии l2 = 50 см. Найти объем шара и зависимость Т(l).
Давление считать постоянным.
5. При какой температуре находился газ в закрытом сосуде, если при нагревании его на ΔT = 140 К
давление возрастает в n = 1,5 раза?
7. В баллоне объемом V = 1,5 л находится воздух при нормальном давлении. За сколько ходов
поршня насоса, имеющего объем цилиндра V1 = 100 см3, можно понизить давление в баллоне в η = 100
раз? Температуру считать постоянной.
8. Компрессор, обеспечивающий работу отбойных молотков, засасывает из атмосферы V0 = 100 л
воздуха в секунду. Сколько отбойных молотков может работать от этого компрессора, если для работы
одного молотка необходимо V = 100 см3 воздуха в секунду при давлении р = 5·106 Па? Атмосферное
давление р0 = 105 Па.
9. Во сколько раз изменится давление в резервуаре пневматического тормоза трамвайного вагона
после n = 250 ходов поршня насоса, если объем резервуара V = 30 л? Насос за одно качание подает
26
ΔV = 600 см3 воздуха при нормальном атмосферном давлении. Изменением температуры пренебречь.
Начальное давление в резервуаре равно нормальному атмосферному давлению.
10. За сколько ходов поршня насоса с рабочим объемом ΔV можно повысить давление от
атмосферного р0 до р в сосуде объемом V? Изменением температуры пренебречь.
11. Начальное состояние газа р0, V0, T0. Газ подвергли сначала изобарическому расширению до
объема Vl, после чего нагрели при постоянном объеме до давления р1. Найти температуру газа в
конечном состоянии.
12. В цилиндрическом сосуде с газом находится в равновесии тяжелый поршень (см.
рис.). Масса газа и температура под поршнем и над ним одинаковы. Отношение объема над
поршнем к объему под поршнем равно 3. Каким будет это отношение, если температуру в
сосуде увеличить в 2 раза?
13. В закрытом сосуде цилиндрической формы находится газ при температуре tl = 0°С. Внутри сосуд
перегорожен легким, не проводящим тепло поршнем радиуса r = 2 см на две части объемами V1 = 10 см3
и V2 = 50 см3. Поршень находится в равновесии. На какое расстояние переместится поршень, если
большую часть газа нагреть на 30 К? Температура в другой части не меняется.
14. График процесса, происходящего с одним молем идеального газа, показан на
рисунке. Участки 2−3 и 1−4 − изотермы. Изобразить график этого процесса в
координатах Т, V. Найти объем V3, если V1 и V2 = V4 заданы.
15. Процесс в идеальном газе идет так, что давление и объем связаны равенством p V = B . Когда
температура газа достигает значения Т, процесс продолжается при другом характере зависимости
Найти температуру Т, считая константы В и D, а также ν количество молей
газа известными.
16. В координатах p, V задан цикл 1−2−3−1 (см. рис.). Изобразить этот цикл в
координатах ρ, Т. Ρ − плотность газа, процесс 3−1 − изотермический. Ответ обосновать.
17. Один моль идеального газа расширяется изобарически. При этом оказалось, что
α = V/T = 2,8·10−3 м3/К. Определить концентрацию молекул газа при температуре Т1 = 103 К.
19. Аэростат объемом V = 300 м3 наполняется молекулярным водородом при температуре Т = 300 К
и давлении p = 105 Па. Какое время будет производиться наполнение оболочки аэростата, если из
баллонов каждую секунду переходит в аэростат Δm = 25 г водорода? До наполнения газом оболочка
аэростата водорода не содержала; газ считать идеальным.
20. Закрытый сосуд объемом V = 10 см3 имеет трещину, через которую ежесекундно проникает
ΔN = 106 частиц газа. Какое время понадобится для наполнения сосуда до нормального давления
р = 105 Па, если скорость проникновения частиц остается постоянной и начальное давление в сосуде
р0 = 0? Температура сосуда с газом Т = 273 К.
21. Цилиндрический сосуд длиной l = 85 см разделен на две части легкоподвижным
поршнем (см. рис.). При каком положении поршня давление в обеих частях цилиндра будет
одинаково, если одна часть заполнена кислородом, а другая водородом такой же массы?
Температура в обеих частях цилиндра одинакова.
22. Какое давление воздуха должно быть в сосуде, объем которого V = 10 л, чтобы при соединении
его с сосудом объемом V2 = 30 л, в котором находится воздух при давлении р2 = 105 Па, установилось
давление р = 3·105 Па? Температуру считать постоянной.
23. В сосуде объемом V1 находится одноатомный газ при давлении p1 и температуре T1, а в сосуде
объемом V2 такой же газ при давлении р2 и температуре Т2. Какое давление и температура установятся в
сосудах при их соединении? Теплообменом с окружающей средой и стенками сосудов пренебречь.
24. Приближенно воздух можно считать смесью азота (η1 = 80% по массе), кислорода (η2 = 16%) и
углекислого газа (η3 = 4%). Найти эффективную молярную массу М воздуха, т. е. молярную массу
такого газа, который при одинаковых параметрах со смесью будет иметь ту же массу.
25. В сосуде при давлении р = 105 Па и температуре t = 27°С находится смесь азота, кислорода и
гелия, массы которых равны. Найти плотность смеси газов.
26. Плотность газа, состоящего из смеси гелия и аргона, ρ = 2 кг/м3 при давлении р = 150 кПа и
температуре t = 27°С. Сколько атомов гелия содержится в газовой смеси объемом V = 1 см3?
27. Сосуд разделен пополам полупроницаемой перегородкой. Объем каждой части V = 1 л. В левую
половину введены водород массой m1 = 2 г и азот массой m2 = 28 г. Справа от перегородки − вакуум.
Какие давления установятся в обеих частях сосуда, если перегородка пропускает только водород, а
температура остается постоянной Т = 373 К?
28. Закрытый сосуд разделен на две равные половины поршнем, который может перемещаться без
трения. Давление и температура в обеих половинах одинаковы. В левой части находится чистый газ 1, в
правой − смесь газов 1 и 2, причем их парциальные давления равны. В некоторый момент поршень
становится проницаемым для газа 2. Во сколько раз η увеличится объем левой части после того, как
установится равновесие?
29. Некоторое количество водорода находится при температуре T1 = 200 К и давлении p1 = 400 Па.
Газ нагревают до температуры Т2 = 104 К, при которой молекулы водорода полностью распадаются на
атомы. Определить давление газа, если его объем и масса не изменились.
30. В сосуде находится озон (O3) при температуре t1 = 527°С. Через некоторое время он полностью
превращается в кислород (O2), температура устанавливается t2 = 127°С. На сколько процентов
изменилось давление в баллоне?
Изопроцессы - МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ
Цель урока: рассмотреть частные случаи закона Клапейрона.
I. Проверка домашнего задания. Повторение изученного
1. Каковы нормальные условия для идеального газа?
2. Какова концентрация молекул идеального газа при нормальных условиях?
3. Какие макроскопические параметры связывает уравнение Клапейрона-Менделеева?
4. Какие параметры необходимо знать для определения состояния идеального газа?
II. Самостоятельная работа
1. Как изменится давление идеального одноатомного газа при уменьшении его объема в 4 раза и увеличении абсолютной температуры в 2 раза?
А. Увеличится в 8 раз.
Б. Увеличится в 4 раза.
В. Увеличится в 2 раза.
2. Вычислите давление кислорода массой 0,032 кг в сосуде объемом 8,3 м 3 при температуре 100 °С.
3. Как меняется масса воздуха в помещении, если температура увеличивается?
В. Не изменяется.
4. Чему равен объем 1 моля идеального газа при нормальных условиях?
5. В баллоне находится газ при t = 27 °С. Во сколько раз уменьшится давление газа, если 50 % его выйдет из баллона, а температура при этом увеличится до 600 К?
6. Масса кислорода m при давлении Р занимает объем V. Как изменится температура газа, если при увеличении давления до 2Р его объем уменьшился в V/10?
A. Увеличится в 5 раз.
Б. Уменьшится в 5 раз.
7. В баллоне при неизменной массе газа температура увеличилась от 1 до 2 °С. Как изменилось давление?
A. Увеличилось в 2 раза.
Б. Увеличилось в 1,004 раза.
B. Не изменилось.
8. Что и по каким физическим величинам можно вычислить на основании уравнения Менделеева-Клапейрона?
1. Плотность газа, используя R, р, Т, М.
2. Число молекул в газе, используя V, Т, Р, с.
3. Массу молекулы, используя Т, Р, с, NA, R.
1. Как изменится давление идеального одноатомного газа при увеличении его объема и температуры в 2 раза?
A. Увеличится в 4 раза.
Б. Уменьшится в 2 раза.
B. Останется прежним.
2. Вычислите давление водорода массой 0,02 кг в сосуде объемом 8,3 м 3 при температуре 100 °С.
3. Как изменится плотность воздуха в помещении, если температура уменьшится?
4. Чему равны давление и температура газа при нормальных условиях?
A. р = 10 5 Па·t – 100 °С 1 м 3 .
Б. р = 10 5 Па·Т - 273 К.
B. р = 10 5 кПа·T - 273 К.
5. В баллоне находится газ при Т = 300 К. Во сколько раз уменьшится давление газа, если 50 % его выйдет из баллона, а температура останется неизменной?
A. Уменьшится в 50 раз.
Б. Уменьшится в 2 раза.
B. Увеличится в 2 раза.
6. При нормальных условиях плотность кислорода:
A. Больше плотности водорода.
Б. Меньше плотности водорода.
B. Равна плотности водорода.
7. При повышении температуры в комнате меняется:
Б. Давление и масса воздуха.
B. Масса воздуха.
8. В цилиндре с поршнем произошло увеличение давления газа больше допустимого за счет увеличения температуры. Как можно установить прежнее давление?
A. Увеличением объема цилиндра или уменьшением массы газа.
Б. Только уменьшением массы газа.
B. Только увеличением объема цилиндра.
Ответы к самостоятельной работе
Ответы и номера вопросов
III. Изучение нового материала
Если одновременно меняются все характеристики состояния газа, то трудно установить какие-либо закономерности. Прошу изучить процессы, в которых масса и один из трех параметров - р, V или Т остаются неизменными.
Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами.
Первый газовый закон был открыт английским ученым Р. Бойлем (1627- 1691 гг.) в 1600 г. Работа называлась «Новые эксперименты, касающиеся воздушной пружины». Бойль изучал изменение давления газа в зависимости от объема при постоянной температуре. Данный процесс называется изотермическим.
Независимо от Бойля несколько позднее французский ученый Э. Мариотт пришел к тем же выводам. Поэтому закон получил название Бойля-Мариотга.
Закон Гей-Люссака (1802 г.)
Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным.
Объем данной массы газа при p = const зависит от температуры по лин. закону
Закон Ж. Шарля (1787 г)
При V = const давление данной массы газа при постоянном объеме зависит от температуры по линейному закону:
Фронтальное экспериментальное задание 1
«Наблюдение зависимости объема данной массы газа от температуры при постоянном давлении»
Приборы и материалы: 1) пробирка химическая, закрытая пробкой со стеклянной трубной длиной 150-200 мм, диаметром 4-5 мм; 2) стакан низкий с водой.
1. Подготовьте оборудование для опыта. Для этого опустите конец трубки с пробкой в стакан с водой на глубину 3-4 см, закройте пальцем другой конец и выньте трубку из воды. Расположите трубку горизонтально. Осторожно закройте пробирку пробкой так. чтобы столбик воды не вылился из трубки.
2. Нагрейте воздух в пробирке, подержав ее несколько секунд в руке. При этом наблюдайте за положением столбика воды в трубке.
3. Прекратите нагревание воздуха в пробирке и снова в течение нескольких секунд, наблюдайте за изменением положения столбика воды в трубке.
4. Ответьте на вопросы:
- Зависимость между какими величинами вы наблюдали на опыте?
- Изменялись ли давление и масса воздуха в пробирке во время опыта?
- Что можно сказать о зависимости объема данной массы воздуха от температуры при постоянном давлении?
Фронтальное экспериментальное задание 2
«Наблюдение зависимости давления данной массы газа от температуры при постоянном объеме»
Уравнение Менделеева – Клапейрона (страница 4)
В сосуде объёмом 2 л находится 10 г идеального газа при давлении 1 атм. и температуре 300 К. Во втором сосуде объёмом 4 л находится 20 г того же газа при давлении 2 атм. Чему равна температура газа во втором сосуде? (Ответ дайте в кельвинах.)
Уравнение состояния газа: \[pV=\nu RT=\dfrac
Для первого сосуда: \[p_1V_1=\dfrac
При уменьшении абсолютной температуры газа на 300 К давление уменьшилось в 5 раз. Какова начальная температура газа, если в ходе эксперимента количество вещества уменьшилось втрое, а объём оставался постоянным? (Ответ дайте в кельвинах.)
Запишем уравнение Менделеева-Клапейрона для первого и второго состояния: \[\begin
Поделив одно уравнение на другое, получим: \[\dfrac
На графиках приведены зависимости давления \(p\) и объема \(V\) от времени \(t\) для 1 моля идеального газа. Чему равна температура газа в момент \(t\) = 30 минут? (Ответ дайте в градусах Кельвина с точностью до 10 К.)
Уравнение состояния идеального газа: \[\displaystyle pV=\nu RT,\] где \(p\) —давление газа, \(V\) —объем газа, \(\nu\) — количество вещества газа, \(R\) — универсальная газовая постоянная, \(T\) — температура. Выразим температуру газа: \[T=\dfrac
\(p=1,2\cdot10^5\) Па
\(V=8,3\cdot10^<-3>\text< м$^3$>\)
Подставим известные и найденные значения в формулу: \[T=\dfrac<1,2\cdot10^5\text< Па>\cdot8,3\cdot10^<-3>\text< м$^3$>><1\text< моль>\cdot8,31\text< >\dfrac<\text<Дж>><\text<моль>>> \approx 120 \text< К>\]
В сосуде неизменного объёма находится разреженный газ в количестве 3 моль. Во сколько раз изменится давление газа в сосуде, если выпустить из него 1 моль газа, а абсолютную температуру газа уменьшить в 2 раза?
Запишем уравнение Клапейрона – Менделеева: \[p1V=\nu_1RT_1=3RT_1\] \[p_2V=\nu_2RT_2=2R\dfrac
Тепловое расширение. Газовые законы
В два сосуда конической формы, расширяющихся кверху и книзу, и цилиндрический налита вода при температуре T = 100 °C. Как изменится давление на дно сосудов после охлаждения воды до комнатной температуры?
В сосуде конической формы, расширяющемся кверху, давление на дно увеличится. В сосуде конической формы, расширяющемся книзу, давление на дно уменьшится. В цилиндрическом сосуде давление на дно не изменится.
Две линейки — одна медная, другая железная — наложены одна на другую так, что они совпадают только одним концом. Определить длины линеек при t = 0 °C, зная, что разность их длин при любой температуре составляет Δl = 10 см. Коэффициент линейного расширения меди α1 = 17·10 -6 К -1 , железа — α2 = 12·10 -6 К -1 .
Длина медной линейки 24 см, длина железной — 34 см.
Часы, маятник которых состоит из груза малых размеров и легкой латунной нити, идут правильно при 0 °C. Найти коэффициент линейного расширения латуни, если при повышении температуры до t = +20 °C часы отстанут за сутки на 16 с.
На сколько часы будут уходить вперед за сутки при t0 = 0 °C. если они выверены при t = 20 °C, и материал, из которого сделан маятник, имеет коэффициент линейного расширения α = 0,000012 К -1 ?
При t0 = 0 °С часы спешат в сутки на τ = 20 с. При какой температуре часы будут идти точно? Коэффициент линейного расширения материала маятника α = 1,9·10 -5 К -1 .
Какую силу F надо приложить к стальному стержню сечением S = 1 см 2 , чтобы растянуть его на столько же, на сколько он удлиняется при нагревании на Δt = 1 °С? Коэффициент линейного расширения α = 12·10 -6 К -1 . Модуль Юнга E = 2,1·10 11 Н/м 2 .
Толщина биметаллической пластинки, составленной из одинаковых полосок стали и цинка, равна d = 0,1 см. Определить радиус кривизны r пластинки при повышении температуры на Δt = 11 °С. Коэффициент линейного расширения цинка α1= 25·10 -6 К -1 , а стали α2 = 12·10 -6 К -1 .
Концы стального стержня сечением S = 1 см 2 , находящегося при температуре t = 20 °С, прочно закреплены. С какой силой стержень будет действовать на опоры, если его нагреть до t1 = 200 °С? Модуль Юнга стали E = 2,0·10 11 Н/м 2 , коэффициент линейного расширения α =1,2·10 -5 К -1 ?
F = 39600 Н.
Каково давление газа p0 в электрической лампочке, объем которой V = 1 л, если при отламывании кончика последней под поверхностью воды на глубине h = 1 м в лампочку вошло m = 998,7 г воды? Атмосферное давление нормальное.
Стеклянный баллон объемом V = 1 л был наполнен испытуемым газом до давления p = 10 5 Па и взвешен. Его вес оказался равным Q = 0,9898 Н. Затем часть газа была удалена так, что давление в баллоне упало до р1 = 5·10 4 Па. Новый вес баллона оказался равным Q1 = 0,9800 Н. Какова плотность испытуемого газа при нормальном атмосферном давлении? Температура постоянна.
ρ = 2,1 кг/м 3 .
p1 = 751 мм рт. ст.
Открытую стеклянную трубку длиной l = 1 м наполовину погружают в ртуть. Затем трубку закрывают пальцем и вынимают. Какой длины столбик ртути останется в трубке? Атмосферное давление равно H = 750 мм рт. ст.
В запаянной с одного конца стеклянной трубке длиной l = 90 см находится столбик воздуха, запертый сверху столбиком ртути высотой h = 30 см; столбик ртути доходит до верхнего края трубки. Трубку осторожно переворачивают открытым концом вниз, причем часть ртути выливается. Какова высота столбика ртути, которая останется в трубке, если атмосферное давление H = 750 мм рт. ст.?
В сосуд со ртутью опускают открытую стеклянную трубку, оставляя над поверхностью конец длиной l = 60 см. Затем трубку закрывают и погружают еще на 30 см. Определить высоту столба воздуха в трубке. Атмосферное давление p0 = 760 мм рт. ст.
.
Посередине откачанной и запаянной с обоих концов горизонтальной трубки длиной L = 1 м находится столбик ртути длиной h = 20 см. Если трубку поставить вертикально, столбик ртути сместится на l = 10 см. До какого давления была откачана трубка? Плотность ртути ρ = 1,36·10 4 кг/м.
Расположенная горизонтально запаянная с обоих концов стеклянная трубка разделена столбиком ртути, на две равные части. Длина каждого столбика воздуха 20 см. Давление 750 мм рт. ст. Если трубку повернуть вертикально, ртутный столбик опускается на 2 см. Определить длину столбика ртути.
Цилиндрический сосуд делится на две части тонким подвижным поршнем. Каково будет равновесное положение поршня, когда в одну часть сосуда помещено некоторое количество кислорода, в другую — такое же по массе количество водорода, если длина сосуда l = 85 см?
В закрытом цилиндрическом сосуде с площадью основания S находится газ, разделенный поршнем массой M на два равных отсека. Масса газа под поршнем при этом в k раз больше массы газа над ним. Температуры газов одинаковы. Пренебрегая трением и массой газа по сравнению с массой поршня, найти давление газа в каждом отсеке.
; .
Имеются два мяча различных радиусов, давление воздуха в которых одинаково. Мячи прижимают друг к другу. Какой формы будет поверхность соприкосновения?
Выгнута в сторону мяча с большим радиусом.
Найти число n ходов поршня, которое надо сделать, чтобы поршневым воздушным насосом откачать воздух из сосуда емкостью V от давления p0 до давления p, если емкость насоса ΔV.
.
Упругость воздуха в сосуде равна 97 кПа. После трех ходов откачивающего поршневого насоса упругость воздуха упала до 28,7 кПа. Определить отношение объемов сосуда и цилиндра насоса.
Два баллона соединены трубкой с краном. В первом находится газ при давлении p = 10 5 Па, во втором — при p1 = 0,6·10 5 Па. Емкость первого баллона V1 = 1 л, второго — V2 = 3 л. Какое давление установится в баллонах (в мм рт. ст.), если открыть кран? Температура постоянная. Объемом трубки можно пренебречь.
Три баллона емкостями V1 = 3 л, V2 = 7 л и V3 = 5 л наполнены соответственно кислородом (p1 = 2·10 5 Па), азотом (p2 = 3·10 5 Па) и углекислым газом (p3 = 6·10 4 Па), при одной и той же температуре. Баллоны соединяют между собой, причем образуется смесь той же температуры. Каково давление смеси?
На гладком горизонтальном столе находится сосуд, разделенный перегородкой на две равные части. В одной части сосуда находится кислород, а в другой — азот. Давление азота вдвое больше давления кислорода. На сколько сдвинется сосуд, если перегородка станет проницаемой? Длина сосуда l = 20 см. Массой сосуда пренебречь. Процесс считать изотермическим.
В цилиндре, закрытом легко подвижным поршнем массой m и площадью S, находится газ. Объем газа равен V. Каким станет объем газа, если цилиндр передвигать вертикально с ускорением: а) +a; б) -a? Атмосферное давление равно p0, температура газа постоянна.
а) ; б) .
Начертить графики изотермического, изобарического и изохорического процессов в идеальном газе в координатах p, V; p, T; V, T. Объяснить, почему коэффициент объемного расширения идеальных газов равен термическому коэффициенту давления.
На рисунке изображены две изотермы одной и той же массы газа.

1. Чем отличаются состояния газов, если газы одинаковы?
2. Чем отличаются газы, если температуры газов одинаковы?
Как менялась температура идеального газа — увеличивалась или уменьшалась — при процессе, график которого в координатах p, V изображен на рисунке.

При нагревании газа получен график зависимости давления от абсолютной температуры в виде прямой, продолжение которой пересекает ось p в некоторой точке выше (ниже) начала координат. Определить, сжимался или расширялся газ во время нагревания.
На рисунке дан график изменения состояния идеального газа в координатах p, V.

Представить этот круговой процесс (цикл) в координатах p, T и V, T, обозначив соответствующие точки.
Сколько ртути войдет в стеклянный баллончик объемом 5 см 3 , нагретый до t1 = 400 °С, при его остывании до t2 = 16 °С, если плотность ртути при t = 16 °С равна ρ = 13,6 г/см 3 ?

При какой температуре находился газ, если при нагревании его на Δt = 22 °С при постоянном давлении объем удвоился? Для каких газов это возможно?
До какой температуры нужно нагреть воздух, взятый при t = 20 °С, чтобы его объем удвоился, если давление останется постоянным?
Определить, каким был бы коэффициент объемного расширения идеального газа, если бы за начальный объем его принимали объем не при t0 =0°С, а при t1 = 100 °С?
В цилиндре, площадь основания которого равна S = 100 см 2 , находится воздух при температуре t1 = 12 °С. Атмосферное давление p1 = 101 кПа. На высоте h1 = 60 см от основания цилиндра расположен поршень. На сколько опустится поршень, если на него поставить гирю массой m = 100 кг, а воздух в цилиндре при этом нагреть до t2 = 27 °С? Трение поршня о стенки цилиндра и вес самого поршня не учитывать.
Два одинаковых баллона, содержащие газ при t = 0 °С, соединены узкой горизонтальной трубкой диаметром d = 5 мм, посередине которой находится капелька ртути.

Капелька делит весь сосуд на два объема по V = 200 см 3 . На какое расстояние x переместится капелька, если один баллон нагреть на Δt = 2 °С, а другой на столько же охладить? Изменением объемов сосудов пренебречь.
Два одинаковых сосуда соединены трубкой, объемом которой можно пренебречь. Система наполнена газом и находится при абсолютной температуре T. Во сколько раз изменится давление в такой системе, если один из сосудов нагреть до абсолютной температуры T1, а другой поддерживать при прежней температуре T?
1. В горизонтально расположенном сосуде, разделенном легко подвижным поршнем, находятся с одной стороны от поршня m1 граммов кислорода, а с другой — m2 граммов водорода. Температуры газов одинаковы и равны T0. Каким будет отношение объемов, занимаемых газами, если температура водорода останется равной T0, а кислород нагреется до температуры T1?
2. Вертикально расположенный сосуд разделен на две равные части тяжелым теплонепроницаемым поршнем, который может скользить без трения. В верхней половине сосуда находится водород при температуре T и давлении p. В нижней части — кислород при температуре 2T. Сосуд перевернули. Чтобы поршень по-прежнему делил сосуд на две равные части, пришлось охладить кислород до температуры T/2. Температура водорода осталась прежней. Определить давление кислорода в первом и втором случаях.
На некоторой высоте давление воздуха p = 3·10 4 Па, а температура t = -43 0 С. Какова плотность воздуха на этой высоте?
Определить давление кислорода, масса которого m = 4 кг, заключенного в сосуд емкостью V = 2 м 3 , при температуре t = 29 °С.
Определить удельный объем азота при температуре 27 °С и давлении p = 4,9·10 4 Па.
Определить массу кислорода, заключенного в баллоне емкостью V = 10 л, если при температуре t = 13 °С манометр на баллоне показывает давление p = 9·10 6 Па.
Какова разница в массе воздуха, заполняющего помещение объемом V = 50 м 3 , зимой и летом, если летом температура помещения достигает t1 = 40 °С, а зимой падает до t2 = 0 °С? Давление нормальное.
Сколько молекул воздуха выходит из комнаты объемом V0 = 120 м 3 при повышении температуры от t1 = 15 °С до t2 = 25 °С? Атмосферное давление p0 = 10 5 Па.
Компрессор захватывает при каждом качании V0 = 4 л воздуха при атмосферном давлении p = 10 5 Па и температуре t0 = -3 °С и нагнетает его в резервуар емкостью V = 1,5 м 3 , причем температура воздуха в резервуаре держится около t1 = 45 °С. Сколько качаний должен сделать компрессор, чтобы давление в резервуаре увеличилось на Δp = 1,96·10 5 Па?
На весах установлены два одинаковых сосуда. Один заполнен сухим воздухом, другой — влажным (насыщенный водяными парами) при одинаковых давлениях и температурах. Какой из сосудов тяжелее?
По газопроводу течет углекислый газ при давлении p = 5·10 5 Па и температуре t = 17 °С. Какова скорость движения газа в трубе, если за τ = 5 мин через площадь поперечного сечения трубы S = 6 см 2 протекает m = 2,5 кг углекислого газа?
Из баллона со сжатым водородом емкостью V = 10 л вследствие неисправности вентиля утекает газ. При температуре t1 = 7 °С манометр показывал p = 5·10 6 Па. Через некоторое время при температуре t2 = 17 °С манометр показал такое же давление. Сколько утекло газа?
Какая часть газа осталась в баллоне, давление в котором было равно p = 1,2·10 7 Па, а температура t = 27 °С, если давление упало до p1 = 10 5 Па? Баллон при этом охладился до t1 = -23 °С.
До какой температуры нужно нагреть запаянный шар, содержащий m = 17,5 г воды, чтобы шар разорвался, если известно, что стенки шара выдерживают давление 10 7 Па, а объем шара V = 1 л?
В цилиндре объемом V, заполненном газом, имеется предохранительный клапан в виде маленького цилиндрика с поршнем. Поршень упирается в дно цилиндра через пружину жесткости k.

При температуре T1 поршень находится на расстоянии l от отверстия, через которое газ выпускается в атмосферу. До какой температуры T2 должен нагреться газ в цилиндре, для того чтобы клапан выпустил часть газа в атмосферу? Площадь поршня S, масса газа в цилиндре m, его молярная масса µ. Объем цилиндрика клапана пренебрежимо мал по сравнению с объемом цилиндра.
В баллоне емкостью V = 110 л помещено m1 = 0,8 кг водорода и m2 = 1,6 кг кислорода. Определить давление смеси на стенки сосуда. Температура окружающей среды t = 27 °С.
В сосуде объемом 1 л заключено m = 0,28 г азота. Азот нагрет до температуры T = 1500 °С. При этой температуре α = 30% молекул азота диссоциировано на атомы. Определить давление в сосуде.
В сосуде находится смесь азота и водорода. При температуре T, когда азот полностью диссоциирован на атомы, давление равно p (диссоциацией водорода можно пренебречь). При температуре 2T, когда оба газа полностью диссоциированы, давление в сосуде 3p. Каково отношение масс азота и водорода в смеси?
Оболочка аэростата объемом V = 1600 м 3 , находящегося на поверхности Земли, наполнена водородом на n = 7/8 при давлении p = 101 кПа и температуре t = 15 °С. Аэростат поднялся на некоторую высоту, где давление p1 = 79,3 кПа и температура t1 = 2 °С. Сколько водорода потерял аэростат при своем подъеме в результате расширения газа?
Доказать, что в атмосфере с постоянной температурой независимо от закона изменения давления с высотой подъемная сила воздушного шара с эластичной оболочкой постоянна. Газ из воздушного шара не вытекает. Пренебречь давлением, обусловленным кривизной оболочки.
Решение №30 ЕГЭ по физике
Как изменится температура идеального газа, если увеличить его объем в 2 раза при осуществлении процесса, описываемого формулой pV 4 = const ?
Решение №30 ЕГЭ по физике.
Выразим из уравнения Менделеева-Клапейрона давление p:
Подставим (1) в формулу, описывающую данный процесс:
Следовательно, при увеличении объема в 2 раза температура должна понизиться в 8 раз
№30 ЕГЭ по физике.
На рисунке изображён процесс 1-2-3-4-5, проводимый над 1 молем идеального одноатомного газа.
Вдоль оси абсцисс отложена абсолютная температура Т газа,
а вдоль оси ординат - количество теплоты Q полученное или отданное газом на соответствующем участке процесса.
После прихода в конечную точку 5 весь процесс циклически повторяется с теми же параметрами изменения величин, отложенных на осях.
Найдите КПД этого цикла.
Решение №30 ЕГЭ по физике.
Определим вначале тип цикла, изображённого на рисунке.
На участке 1—2 имеем , следовательно, изотермический процесс, при котором рабочее тело - газ - получает количество теплоты .
Аналогичным образом, участок 3—4 - это изотермический процесс , при котором рабочее тело отдаёт количество теплоты ,
причём . На участках 2-3 и 4-5 имеем
Таким образом, данный циклический процесс - это цикл идеальной тепловой машины, состоящий из двух изотерм и двух адиабат.
Этот цикл проводится, как видно из рисунка, между максимальной температурой
и минимальной температурой
КПД таког цикла Карно равен
Ответ. КПД цикла равен .
№30 ЕГЭ по физике.
В цилиндре, закрытом подвижным поршнем, находится одноатомный газ,
который может просачиваться сквозь зазор вокруг поршня.
В опыте по изотермическому сжатию газа его объём уменьшился вдвое,
а давление газа упало в 3 раза.
Во сколько раз изменилась внутренняя энергия газа в цилиндре?
Газ считать идеальным.
Решение №30 ЕГЭ по физике.
Внутренняя энергия одноатомного идеального газа пропорциональна
его температуре и числу молей газа: U = (3/2)vRT.
Запишем уравнение Клапейрона–Менделеева:
pV = vRT
(p – давление газа, V – объём сосуда, R – газовая постоянная,
T – температура газа, v – число молей газа).
Из него видно, что произведение vT пропорционально произведению pV.
Значит, согласно условию задачи, внутренняя энергия газа
(как и произведение pV) уменьшилась в 6 раз.
Изопроцессы
Новая тема. И названа она каким-то непонятным словом: изопроцессы. На самом деле – всё не так и сложно. По сути, тема «изопроцессов» – это продолжение темы «Уравнение Клапейрона-Менделеева» . В этом разделе будет идти речь о том, как применять уравнение Клапейрона-Менделеева p V = m M R T pV = \frac
- «изо» – от древнегреческого слова isos – что значит «одинаковый»;
- процесс – значит, что-то происходит, что-то меняется.
Итак, изопроцесс – это процесс изменения чего-то, но при этом изменении что-то другое остаётся неизменным. Что же не меняется в изопроцессах?
- давление газа p p p ;
- объём газа V V V ;
- температура газа T T T .
Если какая-то из этих величин не меняется, в то время как две другие величины меняются – то мы имеем дело с «изопроцессом».
Существует три типа изопроцессов:
- не меняется давление газа p p p – изобарный процесс: p = c o n s t p = const p = c o n s t .
- не меняется объём газа V V V – изохорный процесс: V = c o n s t V = const V = c o n s t .
- не меняется температура газа T T T – изотермический процесс: T = c o n s t T = const T = c o n s t .
Поэтому особое значение имеют процессы, в которых что-то неизменно, то есть процессы с одной постоянной величиной – «изопроцессы». В таких процессах меньше «хаоса» и «непонятности».
Разберём каждый из изопроцессов подробнее. Для наглядности будем рассматривать сосуд с некоторым газом – например, гелием. В верхней части сосуда – пусть будет поршень, который мы можем двигать или который может двигаться самостоятельно.
1. Изобарный процесс : p = c o n s t p = const p = c o n s t .
При изобарном процессе неизменно давление.
Как в реальности можно сделать так, чтобы давление газа не изменялось? (Учтите, что правильным является только один вариант ответа.)
Держать газ при постоянной температуре; не давать ему охлаждаться и нагреваться.
Держать газ в плотно закрытой ёмкости, объём которой неизменен.
Поместить газ под поршень постоянной массы, который может свободно двигаться.
Изобарный процесс – это идеализация; в реальности сделать его невозможно.
Представим, что мы нагрели наш газ, находящийся под поршнем – то есть находящийся при постоянном давлении. Пусть исходное состояние обозначается цифрой 1 1 1 , а конечное – цифрой 2 2 2 .
Тогда для первого состояния мы можем записать: p V 1 = m M R T 1 pV_1 = \frac
Во сколько раз изменится давление газа в цилиндре
С1-1. На полу неподвижного лифта стоит теплоизолированный сосуд, открытый сверху. В сосуде под тяжёлым подвижным поршнем находится одноатомный идеальный газ. Поршень находится в равновесии. Лифт начинает равноускоренно опускаться вниз. Опираясь на законы механики и молекулярной физики, объясните, куда сдвинется поршень относительно сосуда после начала движения лифта и как при этом изменится температура газа в сосуде. Трением между поршнем и стенками сосуда, а также утечкой газа из сосуда пренебречь.
С1-2. В цилиндре, закрытом подвижным поршнем, находится идеальный газ. На рисунке показана диаграмма, иллюстрирующая изменение внутренней энергии U газа и передаваемое ему количество теплоты Q. Опишите изменение объема газа при его переходе из состояния 1 в состояние 2, а затем в состояние 3. Свой ответ обоснуйте, указав, какие физические закономерности вы использовали для объяснения.
С1-2. В цилиндре, закрытом подвижным поршнем, находится идеальный газ. На рисунке показана диаграмма, иллюстрирующая изменение внутренней энергии U газа и передаваемое ему количество теплоты Q. Опишите изменение объема газа при его переходе из состояния 1 в состояние 2, а затем в состояние 3. Свой ответ обоснуйте, указав, какие физические закономерности вы использовали для объяснения.
С1-3. В цилиндре, закрытом подвижным поршнем, находится газ, который может просачиваться сквозь зазор вокруг поршня. В опыте по изотермическому сжатию газа его объем уменьшился вдвое, а давление газа упало в 3 раза. Во сколько раз изменилась внутренняя энергия газа в цилиндре? (Газ считать идеальным.)
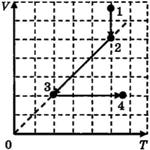
C1-5. Ha V T-диаграмме показано, как изменялись объём и температура некоторого постоянного количества разреженного газа при его переходе из начального состояния 1 в состояние 4. Как изменялось давление газа р на каждом из трёх участков 1—2, 2—3, 3—4: увеличивалось, уменьшалось или же оставалось неизменным? Ответ поясните, указав, какие физические явления и закономерности вы использовали для объяснения.
C1-6. В цилиндрическом сосуде под поршнем длительное время находятся вода и ее пар. Поршень начинают выдвигать из сосуда. При этом температура воды и пара остается неизменной. Как будет меняться при этом масса жидкости в сосуде? Ответ поясните, указав, какие физические закономерности вы использовали для объяснения.
С3-9. Нагреваемый при постоянном давлении идеальный одноатомный газ совершил работу 400 Дж. Какое количество теплоты было передано газу?
С3-11. В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 8 раз, давление воздуха в сосуде увеличилось в 2 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
С3-12. В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 4 раза, давление воздуха в сосуде увеличилось тоже в 4 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
С3-13. С разреженным азотом, который находится в сосуде под поршнем, провели два опыта. В первом опыте газу сообщили, закрепив поршень, количество теплоты Q1 = 742 Дж, в результате чего его температура изменилась на некоторую величину ΔT. Во втором опыте, предоставив азоту возможность изобарно расширяться, сообщили ему количество теплоты Q2 = 1039 Дж, в результате чего его температура изменилась также на ΔT. Каким было изменение температуры ΔT в опытах? Масса азота m = 1 кг.
С3-14. С разреженным азотом, который находится в сосуде под поршнем, провели два опыта. В первом опыте газу сообщили, закрепив поршень, количество теплоты Q1 = 742 Дж, в результате чего его температура изменилась на 1 К. Во втором опыте, предоставив азоту возможность изобарно расширяться, сообщили ему количество теплоты Q2 = 1039 Дж, в результате чего его температура изменилась также на 1 К. Определите массу азота в опытах.
С3-15. В горизонтальном цилиндрическом сосуде, закрытом поршнем, находится одноатомный идеальный газ. Первоначальное давление p = 4 • 10 5 Па. Расстояние от дна сосуда до поршня L = 30 см. Площадь поперечного сечения поршня S = 25 см 2 . В результате медленного нагревания газа поршень сдвинулся на расстояние х = 10 см. При движении поршня на него со стороны стенок сосуда действует сила трения величиной Fтр = 3•10 3 H. Какое количество теплоты получил газ в этом процессе? Считать, что сосуд находится в вакууме.
С3-16. В горизонтальном цилиндрическом сосуде, закрытом подвижным поршнем, находится одноатомный идеальный газ. Давление окружающего воздуха р = 10 5 Па. Трение между поршнем и стенками сосуда пренебрежимо мало. В процессе медленного охлаждения от газа отведено количество теплоты │Q│ = 75 Дж. При этом поршень передвинулся на расстояние х = 10 см. Чему равна площадь поперечного сечения поршня? Количество вещества газа постоянно.
С3-17. В горизонтальном цилиндрическом сосуде, закрытом поршнем, находится одноатомный идеальный газ. Первоначальное давление газа р1 = 4 · 10 5 Па. Расстояние от дна сосуда до поршня равно L. Площадь поперечного сечения поршня S = 25 см 2 . В результате медленного нагревания газ получил количество теплоты Q = 1,65 кДж, а поршень сдвинулся на расстояние х = 10 см. При движении поршня на него со стороны стенок сосуда действует сила трения величиной Fтp = 3 · 10 3 Н. Найдите L. Считать, что сосуд находится в вакууме.
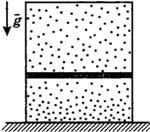
С3-18.Вертикальный замкнутый цилиндрический сосуд высотой 50 см разделен подвижным поршнем весом 110 Н на две части, в каждой из которых содержится одинаковое количество идеального газа при температуре 361 К. Сколько молей газа находится в каждой части цилиндра, если поршень находится на высоте 20 см от дна сосуда? Толщиной поршня пренебречь.
С3-19.В вертикальном теплоизолированном цилиндрическом сосуде под поршнем находится 0,5 моль гелия, нагретого до некоторой температуры. Поршень сначала удерживают, затем отпускают, и он начинает подниматься. Масса поршня 1 кг. Какую скорость приобретет поршень к моменту, когда поршень поднимется на 4 см, а гелий охладится на 20 К? Трением и теплообменом с поршнем пренебречь.
С3-20. Теплоизолированный сосуд объемом V = 2 м 3 разделен теплоизолирующей перегородкой на две равные части. В одной части сосуда находится 2 моль Не, а в другой — такое же количество моль А r . Температура гелия Т1 = 300 К, а температура аргона Т2 = 600 К. Определите парциальное давление аргона в сосуде после удаления перегородки.
Термодинамика С3-21. На рисунке изображено изменение состояния 1 моль идеального одноатомного газа. Начальная температура газа 27° С. Какое количество теплоты сообщено газу в этом процессе?
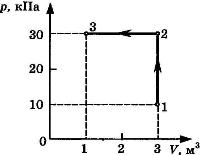
С3-23. На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
С3-24. На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
С3-25. На диаграмме (см. рисунок) представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?
Читайте также:

